
题目列表(包括答案和解析)
2、科学家最近发现2种粒子:第1种是只由四个中子构成的粒子,这种粒子称为“四中子”,
也有人称之为“零号元素”;第2种是由四个氧原子构成的分子。下列有关这两种粒子的说法不正确的是
A、“四中子”不显电性 B、“四中子”的质量数为4
C、第2种粒子是氧元素的另一种同位素 D、第2种粒子的化学式为O4
1、上海环保部门为了使城市生活垃圾得到合理利用,近年来逐步实施了生活垃圾分类投放
的办法。其中塑料袋、废纸、旧橡胶制品等属于
A、 无机物 B、 有机物 C、 盐类 D、 非金属单质
26、某有机物的蒸汽与相同状况下同体积H2的质量比是30,其分子中碳、氢的质量分数分别是40%、6.6%,其余是氧。
(1)求该有机物的分子式;
(2)若该有机物能与Na2CO3溶液反应产生气体,写出其结构简式。
25、(12分)经测定乙醇的化学式是C2H6O,由于有机物普遍存在同分异构现象,推测乙醇的结构可能是下列两种之一。
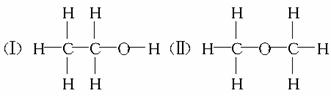
为测定其结构,应利用物质的特殊性进行定性、定量实验。现给出乙醇、钠、水及必要的仪器,请甲、乙、丙三位同学直接利用如图给定装置开始进行实验确定乙醇的结构。
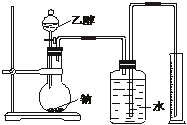
(1)同学甲得到一组实验数据:
|
乙醇的物质的量/mol |
氢气的体积/L |
|
0.10 |
1.12(标准状况) |
根据以上数据推断乙醇的结构为 ▲ (用Ⅰ、Ⅱ表示),理由为 ▲ 。
(2)同学乙分别准确称量4.60 g 乙醇进行多次实验,结果发现以排开量筒内的体积作为生成的H2体积,换算成标准状况后都小于1.12 L,如果忽略量筒本身及乙同学读数造成的误差,那么乙认为可能是由于样品中含有少量水造成的,你认为正确吗? ▲ (填“正确”或“不正确”)。如果你认为不正确,理由是 ▲ (如果你认为正确,此空不填)。
(3)同学丙认为实验成功的关键有:①装置气密性要良好,②实验开始前准确取用乙醇的量,③钠足量,④广口瓶内水必须充满,⑤氢气体积的测算方法正确、数据准确。其中正确的有 ▲ (填序号)。
(4)实验后,同学们从乙醇的可能结构分析入手,对乙醇和钠的量的关系进行了讨论,如果乙醇的物质的量为n mol,那么对钠的物质的量的取值要求必须是 ▲ 。
24.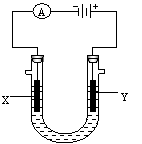 (6分)电解原理在化学工业中有广泛应用。下图表示一个电解池,U型管中装有饱和CuCl2溶液,X、Y是两块惰性电极板,通过导线与直流电源相连。请回答以下问题:
(6分)电解原理在化学工业中有广泛应用。下图表示一个电解池,U型管中装有饱和CuCl2溶液,X、Y是两块惰性电极板,通过导线与直流电源相连。请回答以下问题:
(1)写出电解池中X极发生的电极反应式 ▲ 。
(2)用湿润的淀粉碘化钾试纸检验Y电极反应产物的
现象为 ▲ 。
(3)在化学反应中发生的能量转变形式是 ▲ 。
23、(6分)在2SO2 +
O2 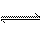 2SO3反应中:如果2分钟内SO2的浓度由6 mol.L-1下降为2 mol.L-1
,那么,2分钟内用SO2浓度变化来表示的化学反应速率为
▲ mol.(L·min)-1,用O2浓度变化来表示的化学反应速率为 ▲ mol.(L·min)-1。此时若保持密闭容器的体积不变,往容器中充入N2使压强增大,则反应速率将 ▲
(填“增大”、“不变”或“减小”)。
2SO3反应中:如果2分钟内SO2的浓度由6 mol.L-1下降为2 mol.L-1
,那么,2分钟内用SO2浓度变化来表示的化学反应速率为
▲ mol.(L·min)-1,用O2浓度变化来表示的化学反应速率为 ▲ mol.(L·min)-1。此时若保持密闭容器的体积不变,往容器中充入N2使压强增大,则反应速率将 ▲
(填“增大”、“不变”或“减小”)。
22、(5分)下图是炭和水蒸汽发生反应生成CO、H2的途径和三个状态的能量,该反应为吸热反应,试问:
(1)步骤1、2分别是吸热过程还是放热过程?步骤1: ▲ ,步骤1: ▲ 。
(2)比较E1、E2、E3的大小: ▲ 。
|
|

|
 步骤1
步骤2
步骤1
步骤2
E1 E2 E3
21、(10分)下表为元素周期表的一部分,请按要求回答问题:
|
族 周期 |
ⅠA |
ⅡA |
ⅢA |
ⅣA |
ⅤA |
ⅥA |
ⅦA |
0 |
|
2 |
① |
|
|
② |
|
③ |
④ |
⑤ |
|
3 |
⑥ |
⑦ |
|
|
|
⑧ |
⑨ |
|
(1)表中元素 ▲ 的非金属性最强,元素 ▲ 的金属性最强(填元素符号)。
(2)表中元素③的原子结构示意图 ▲ ;元素⑨形成的氢化物的电子式 ▲ 。
(3)表中元素④、⑨形成的氢化物的稳定性顺序为 ▲ > ▲ (填化学式)。
(4)表中元素⑧和⑨的最高价氧化物对应水化物的酸性强弱为 ▲ > ▲ (填化学式)。
(5)表中元素③、④、⑥、⑦的原子半径大小为 ▲ > ▲ > ▲ > ▲ (填元素符号)。
20、(8分)(1)某主族元素的最高正化合价为+6,其负化合价为 ▲ 。元素R与氢形成的氢化物的化学式为RH3,其最高价氧化物的化学式为 ▲ 。
(2)硼有无定形和晶体两种,参考下列数据判断:晶体硼属于 ▲ 晶体,理由是 ▲ 。
|
|
金刚石 |
晶体硅 |
晶体硼 |
|
熔点(K) |
>3823 |
1683 |
2573 |
|
沸点(K) |
5100 |
2628 |
2823 |
|
硬度(Moh) |
10 |
7.0 |
9.5 |
19、(9分)写出下列化学方程式,并指出反应类型:
(1)CH4与Cl2光照生成CH3Cl ▲ ,反应类型 ▲ 。
(2)乙烯与水反应 ▲ ,反应类型 ▲ 。
(3)由氯乙烯(CH2=CHCl)合成聚氯乙烯 ▲ ,反应类型 ▲ 。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com