
题目列表(包括答案和解析)
7.关于可逆反应达到平衡的说法错误的是
A.外界条件不能改变平衡 B.正、逆反应速率相等
C.各组分的含量不随时间而变化 D.是动态平衡
6.下列物质属于电解质的是
A.石墨 B.蔗糖 C.稀硫酸 D.NaC1
5.元素R的阴离子Rn-核外有x个电子,其核内的中子数为m,则R的质量数是
A.x-n B.m-x+n C.m+x-n D.x+n
4.0.5mol Na2SO4中所含的Na+离子数为
A.3.01×1023 B.6.02×1023 C.0.5 D.1
3.属同分异构体的是
A.正丁烷与异丁烷 B.16O与18O C.红磷与白磷 D.H2O与D2O
2.下列气态氢化物中最不稳定的是
A. CH4 B. SiH4 C. H2O D. HCl
1.澳大利亚研究人员最近开发出被称为第五形态的固体碳,这种新的碳结构称作“纳米泡沫”,它外形类似海绵,比重极小,并具有磁性。纳米泡沫碳与金刚石的关系是
A.同种物质 B.同分异构体 C.同位素 D.同素异形体
三 本题包括3小题,共27分
21 (14分)(1)温度降低,食物腐败的速率降低 (2)反应物本身的性质;温度、浓度、压强、催化剂 (3) 3, 7, 5
 22 (10分)Fe Fe-2e-==Fe2+
22 (10分)Fe Fe-2e-==Fe2+
石墨或铜片 Cu2++2e-==Cu
氯化铜或硫酸铜溶液
CuSO4溶液
23 (3分)随着元素的原子序数的递增,元素的电负性呈同期性的变化
24 (每空1分,共7分)
(1) ;
; (2)
(2) ;
;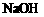 ;
;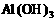 (3)略
(3)略
25
Ⅰ(共7分)
(1)①第三周期元素的氯化物,自钠到硅,键型由离子化合物过渡到共价化合物,沸点显著地降低。(2分) ②SiCl4、AlCl3(2分) ③ ﹥(1分)
Ⅱ (共8分)(1)B (2)Ni(OH)2和Cd(OH)2能溶于酸性溶液。(3)锂的摩尔质量小 :2Li+2H2O = 2LiOH+H2↑
26 (6分)(1)4.8×10-4mol·L-1·s-1(2)图中实践
(3)图中虚线
五 本小题包括1小题,共10分
27 (10分)(1)2Al+6HCl=2AlCl3+3H2↑ (1分)
(2)胶头滴管、温度计 (每空1分)
(5)5mL; 35mL;10mL。
EF>FG>OE; (每空1分)
OE段温度较低,所以此时生成氢气的速率最小;而EF段速率最大,是因为铝与盐酸反应是一个放热反应,反应一段时间后,反应体系温度升高,所以反应速率增大;FG段是由于溶液中氢离子的浓度降低,所以导致了反应速率的减小。 (3分)
六 选做题,本题共8分
28 (8分) ;
;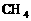 ;
;
29 (每空2分,共8分)
(1) ;
; (2)
(2) ;
;
三 本题包括3小题,共27分
21 (14分)(1) , 、 、 、
。
(2) 。
(3) _______ , , 。
22 (10分) ,
, ,
。
23 (3分)
四 本题包括3小题,共35分
24 (14分)(1) ,
(2) , ,
(3) ,
。
25 Ⅰ(共7分)① 。
② 。
③ LiCl BCl3
Ⅱ(8分)(1)
(2)
(3) ,
。
26 (6分)(1)
 (2)(3)
(2)(3)
五 本小题包括1小题,共10分
27(10分)(1)
(2) ,
(5)② OE: ;EF: ;FG: 。
速率大小比较: ;
原因解释:
。
六 选做题,本题共8分
28 (8分)A: ;B: ;C: 。
29 (8分)(1) ,
(2) ,
高一化学第二学期(专业班)期中考试试题
四 本题包括3小题,共35分
24 (14分)下表是元素周期表的一部分,按要求回答所列有关问题。
|
周期 |
族 |
|||||||
|
ⅠA |
ⅡA |
ⅢA |
ⅣA |
ⅤA |
ⅥA |
ⅦA |
0 |
|
|
2 |
|
|
|
|
① |
|
② |
|
|
3 |
③ |
④ |
⑤ |
⑥ |
|
⑦ |
⑧ |
|
(1)在所示八种元素中,最活泼的非金属元素是 ,最活泼的金属元素是 。(均填元素符号)
(2)在所示八种元素的最高价氧化物对应的水化物中,酸性最强的酸是 ,碱性最强的碱是 ,呈两性的氢氧化物是 。(均填化学式)
(3)用电子式表示③与⑦形成的化合物的形成过程
⑥与⑧形成的化合物的电子式 。
25 Ⅰ (共7分)下表列有四种物质的沸点
|
物质 |
NaCl |
MgCl2 |
AlCl3 |
SiCl4 |
|
沸点/℃ |
1465 |
1412 |
181(升华) |
57.6 |
①从表中的数据,结合学过的化学知识,你能得到的规律是 。
②以上四种物质中,属于共价化合物的是 。
③若你得到的规律具有普遍性,则以下两种物质的沸点高低是:LiCl BCl3(填“>”、“==”、“<”)。
Ⅱ(8分) 化学电池在通讯、交通及日常生活中有着广泛的应用。
(1)目前常用的镍(Ni)镉(Cd)电池,其电池总反应可以表示为:
Cd+2NiO(OH)+2H2O 2Ni(OH)2+Cd(OH)2
2Ni(OH)2+Cd(OH)2
已知Ni(OH)2和Cd(OH)2均难溶于水但能溶于酸,以下说法中正确的是
① 以上反应是可逆反应 ② 以上反应不是可逆反应
③ 充电时化学能转变为电能 ④ 放电时化学能转变为电能
A ①③ B ②④ C ①④ D ②③
(2)废弃的镍镉电池已成为重要的环境污染物,有资料表明一节废镍锡电池可以使一平方米面积的耕地失去使用价值。在酸性土壤中这种污染尤为严重。这是因为 (3)另一种常用的电池是锂电池(是一种碱金属元素,其相对原子质量为7,由于它的比容量(单位质量电板材料所能转换的电量)特别大而广泛应用于心脏起搏器,一般使用时间可长达十年。它的负极用金属锂制成;电池总反应可表示为:Li+MnO2→LiMnO2
试回答:锂电池比容量特别大的原因是 锂电池中的电解质溶液需用非水溶剂配制,为什么这种电池不能使用电解质的水溶液?请用化学方程式表示其原因
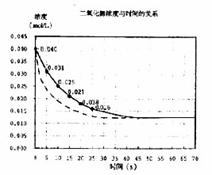
26 (6分)二氧化氮在加热条件下能够分解成一氧化氮和氧气。该反应进行到45秒时,达到平衡(NO2浓度约为0.0125mol/L)。右图中的吗线表示二氧化氮分解反应在前25秒内的反应进程。
 (1)请计算前25秒内氧气的平均生成速率:
(1)请计算前25秒内氧气的平均生成速率:
(2)若反应延续至70秒,请在图中用实线画出25秒至70秒的反应进程曲线。
(3)若在反应开始时加入催化剂(其他条件都不变),请在图上用虚线画出加入催化剂后的反应进程曲线。
五 本小题包括1小题,共10分
27(10分)某课外兴趣小组欲探究铝与盐酸的反应实验中反应速率与哪些因素有关。请填写下列空白:
(1)实验原理: (用化学方程式表示)。
(2)实验用品:试管(普通试管和具支试管各一支)、镊子、乳胶管、玻璃导管、水槽、 、 (填写所缺的实验用品);稀盐酸(4mol/L)、铝条(片)、水
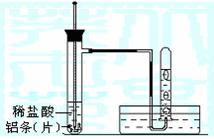 (3)实验装置 (图中铁架台等夹持仪器略去)
(3)实验装置 (图中铁架台等夹持仪器略去)
(4)实验方法
①按如图所示连接好实验仪器,检查装置的气密性。
②取3块铝条加入到试管中。
③在盛有铝条的试管中,加入2mL稀盐酸。
④测量试管中溶液的温度。
⑤收集反应产生的氢气。
(5)数据处理及问题讨论
①实验结束后,课外兴趣小组成员将产生氢气的体积与时间作了如下的图。
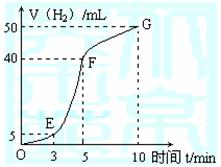
②试判断OE、EF、FG段所收集气体的多少。
OE: ;EF: ;FG: 。
写出这三段时间内产生氢气的速率大小比较(用OE、EF、FG表示),并解释原因。
速率大小比较: ;
原因解释: 。
六 选做题,本题共8分
28 (8分) 下列物质结构图中,●代表原子序数从1到10的元素的原子实(原子实是原子除去最外层电子后剩余的部分),小黑点代表未用于形成共价键的最外层电子,短线代表价键,每共用一对电子用一根短线表示(示例:F2 ):

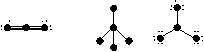
A B C
根据各图表示的结构特点,写出该分子的化学式:
A: ;B: ;C: 。
29 (8分)1919年,Langmuir提出等电子原理:原子数相同、电子总数相同的分子,互称为等电子体。等电子体的结构相似、物理性质相近。
(1)根据上述原理,仅由第2周期元素组成的共价分子中,互为等电子体的是:N2和 ;N2O和 。(填化学式)
(2)此后,等电子原理又有所发展。例如,由短周期元素组成的微粒,只要其原子数相同,各原子最外层电子数之和相同,也可互称为等电子体,它们也具有相似的结构特征。在短周期元素组成的物质中,与 互为等电子体的分子有: 、 。(填化学式)
互为等电子体的分子有: 、 。(填化学式)
高一化学第二学期(专业班)期中考试试题
 第一部分 选择题(共70分)
第一部分 选择题(共70分)
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com