
题目列表(包括答案和解析)
22. (8分)分子个数比为 ,原子个数比为 ,体积比为 ,密度比为 。
21.(8分) 摩/升, 摩/升, 克。 摩/升。
|
1 |
2 |
3 |
4 |
5 |
6 |
7 |
8 |
9 |
10 |
|
|
|
|
|
|
|
|
|
|
|
|
11 |
12 |
13 |
14 |
15 |
16 |
17 |
18 |
19 |
20 |
|
|
|
|
|
|
|
|
|
|
|
28.(6分)取部分被氧化的镁带2.36克溶于60毫升2摩/升的硫酸溶液中,产生气体2.016升(标准状况下),求:
(1) 镁带中剩余镁的质量。
(2) 向反应后的溶液中加入氢氧化钠溶液,若要使沉淀量达到最大值,至少需要加入6摩/升的氢氧化钠溶液多少毫升?
高一年级化学第一学期期中试卷
27.(6分)将26.1克MnO2与500毫升12摩/升的浓盐酸共热,
 反应方程式为:MnO2+4HCl(浓)
反应方程式为:MnO2+4HCl(浓) MnCl2+ Cl2 + 2H2O,则:
MnCl2+ Cl2 + 2H2O,则:
(1) 完全反应后可生成氯气多少升?(标准状况下)
(2) 参加反应的氯化氢的物质的量为多少?
(3) 如果不考虑氯化氢的损失,在反应后的溶液里加入过量的硝酸银溶液,能生成氯化银沉淀多少克?
(四) 问题讨论(均填“偏大”、“偏小”、“无影响”)
(1)若不用蒸馏水洗涤烧杯,则所配溶液的浓度将_______ ,若仪器A用蒸馏水洗后未烘干,则所配溶液的浓度将_______ 。
(2)定容时,俯视观察凹液面最低处与刻度线相切,则所得溶液的浓度将_______ 。
26.(4分)如图所示,烧瓶内充满干燥的氯化氢气体,
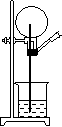 (1)当打开弹簧夹,并挤压预先盛水的胶头滴管后,可以看到
(1)当打开弹簧夹,并挤压预先盛水的胶头滴管后,可以看到
___________________________________________________
产生上述现象的原因是________________________________
(2)若喷泉实验后,水充满整个烧瓶,则所得盐酸物质的量浓度约为 __摩/升。(S.T.P)
(三) 配制:(操作顺序已被打乱)
① 向盛有氢氧化钠的烧杯中加入20毫升水使其溶解;
② 继续向A仪器中加水至液面接近刻度线2-3cm处;
③ 将冷却后的氢氧化钠溶液沿玻璃棒注入A仪器中;
④ 在烧杯中加入少量水洗涤,洗涤液也注入A仪器中,重复2-3次,轻轻摇匀;
⑤改用B仪器加水至刻度线,加盖充分摇匀。
仪器A是__ _____,仪器B是_______ ;
正确的操作顺序是__ ____ 。
(二) 称量:
(一) 计算:需要氢氧化钠固体________。
24.(12分)某学生发现氯水能使有色布条褪色,氯水的成分比较复杂,那么氯水中究竟什么成分具有漂白性呢?带着疑问,他作了如下探究:
⑴查找资料后得知氯水的成分有_________、__________、___________、______________,
⑵实验探究
|
序号 |
方法简述 |
现象和结论 |
|
1 |
|
|
|
2 |
|
|
⑶根据资料查阅和实验结果分析,可推知具有漂白性的物质是________,该物质之所以具有漂白性,与它的____ __性质有关。
⑷该学生的探究活动体现了最基本的科学研究方法,即:

25.(8分)某同学欲配制100毫升、0.2摩/升的氢氧化钠溶液,具体方案如下:
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com