
题目列表(包括答案和解析)
1.“保护环境,就是保护人类自己”。目前,在我国城市环境主要的大气污染物是
A.SO2、NO2、CO、烟尘 B.NH3、CO2、NO、雾
C.HCl、SO2、N2、粉尘 D. CO2、Cl2、N2、酸雨
28.(8分)现有等物质的量的NaHCO3和KHCO3的混合物a(g)与100mL盐酸反应.题中涉及的气体体积均为标准状况下,填空时可以用带字母的分式表示.
(1)该混合物中NaHCO3与KHCO3的质量比为____________.
(2)如碳酸氢盐与盐酸恰好完全反应,则盐酸的浓度为___________mol·L-1.
(3)如盐酸过量,生成CO2的体积为_____________L
(4)如果反应后碳酸氢盐有剩余,盐酸不足量,要计算生成CO2的体积,还须知道______________,说明原因: ___________________________
27.(7分)密闭容器中将3.62 gNaOH、Na2S、Na2SO3的混合物溶于50 mL某浓度的稀 H2SO4
中,不放出任何气体,再加入100 mL 0.1mol·L-1的Ba(OH)2溶液,正好中和过量的
H2SO4。将反应所得沉淀分离、洗净、烘干、称重,其质量为3.29 g 。求:
(1)原混合物中各物质的物质的量之比;
(2)原稀H2SO4的物质的量浓度。
26.(7分)超重元素的假设预言自然界中可能存在114号的稳定同位素X,请根据原子构
理论和元素周期律预测:
(1)X元素位于周期表中第_______周期,________族,为_______元素(金属或非金属)
(2)写出其最高价氧化物及其水化物的化学式_______________、_____________,并估
计后者为_____________(酸性或碱性)
(3)它与氯气反应生成的化合物的化学式为_________________。
25.(12分)1-18号元素A、B、C、D中,0.5molA元素的离子得到6.02×1023个电子被还原为中性原子,0.4gA的氧化物恰好与100mL 0.2mol/L的盐酸完全反应,A原子核内质子数与中子数相等。B元素原子核外M层比K层多1个电子。C得到一个电子后电子层结构达到稳定结构,其最高价氧化物的水化物为自然界最强的酸。D元素原子核外L层比K层多2个电子。
(1)写出A、B、C、D四种元素的符号:
A_______、B_______、C_______ 、D_______
(2)C的离子结构示意图为________;D的原子结构示意图为_______
(3)向10mL浓度为1mol/L的B、C两元素形成的化合物的水溶液里逐滴滴入35ml浓度为1mol/L的苛性钠溶液现象是__________________________________,离子反应方程式为___________________________________。
将生成物过滤、洗涤、干燥灼烧,可得白色固体质量为 。
24.(8分)为了验证浓H2SO4和木炭在加热时发生反应生成水、二氧化碳和二氧化硫。为确认各种产物,甲、乙两学生分别设计如下实验方案:(图中→表示气体流向)
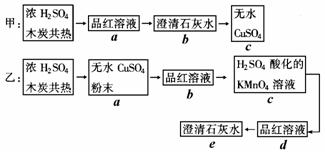
(1)上述甲、乙两方案中可达到实验目的的是______________(填“甲”或“乙”)。
(2)简述方案不可行的理由__________________________________________________
(3)具体说明能达到实验目的的方案中,气体通过的各装置(用字母表示)的作用:_____________________________________________________________________
23.(6分)溴化碘(IBr)的化学性质类似于卤族单质,试回答下列问题:
(1)IBr的电子式_____________,IBr属 ______化合物。(填“离子”或“共价”,下同)
(2)溴化碘和金属镁反应生成物属于_______化合物,生成物之一的电子式 。
(3)溴化碘和水反应生成一种三原子分子,该分子的电子式为__________,其分子中化学键类型为___________。
22.(8分)现有以下物质:①NaCl晶体 ②液态SO3 ③液态的醋酸 ④汞 ⑤BaSO4固体
⑥纯蔗糖(C12H22O11) ⑦酒精(C2H5OH) ⑧熔化的KNO3,请回答下列问题(用序号):
⑴以上物质中能导电的是________________。
⑵以上物质中属于电解质的是__________________。
⑶以上物质中属于非电解质的是__________________。
⑷以上物质中溶于水后形成的水溶液能导电的是___________________。
21.(7分)(1)工业上制造普通玻璃的主要原料是 ___、 ___ 、_________,
主要原料熔化后,发生的主要化学反应是:
(2)____________________________________________;
20.化合物A、B、C都只含两种元素,且A、B均含X元素,已知在一定条件下可发生反应 A+B→X+C,X是一种单质,由此可知X元素 ( )
A.一定是金属元素 B.一定是非金属元素
C.可能是金属元素 D.可能是非金属元素
第ІІ卷
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com