
题目列表(包括答案和解析)
11.关于用水制取二级能源氢气,以下研究方向不正确的是 ( )
A.构成水的氢和氧都是可以燃烧的物质,因此可研究在水不分解的情况下,使氢成为二级
能源; B.设法将太阳光聚焦,产生高温使水分解产生氢气;
C.寻找高效催化剂,使水分解产生氢气
D.寻找特殊化学物质,用于开发廉价能源,以分解水制取氢气
10.有a、b、c、d四种金属,将a与b用导线连结起来浸入电解质溶液中,b不易腐蚀。将a、d分别投入等浓度的盐酸中,d比a反应剧烈。将Cu浸入b的盐溶液里,无明显变化。如果把Cu浸入c的盐溶液里,有c的单质析出,据此判断它们的活动性由强到弱的顺序是 ( )
A.d、c、a、b B.b、a、d、c C.d、b、a、c D.d、a、b、c
9.下图各装置中,可以构成原电池的是 ( )
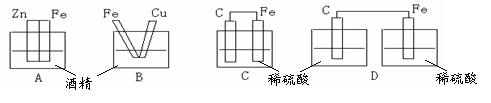
8.下列对热化学方程式1/2H2(g) + 1/2I2(g)==HI(g) △H=+26 kJ·mol-1的叙述正确的
是 ( )
A.1 mol H2(g)和1 mol I2(g)完全反应生成2 mol HI(g)需要吸收26 kJ热量。
B.1个H2(g)分子和1个I2(g)分子完全反应生成2 个 HI(g)需要吸收52 kJ热量。
C.1 mol H2(g)与1 mol I2(g)完全反应生成2 mol HI(g)需吸收52 kJ热量。
D.1 mol H2(g)与1 mol I2(g)完全反应生成2 mol HI(g)放出26 kJ热量。
7.关于吸热反应和放热反应,下列说法错误的是 ( )
A.需要加热才能进行的化学反应一定是吸热反应
B.化学反应中的能量变化,除了热能外,还可以是光能、电能等
C.化学反应过程中的能量变化,也服从能量守恒定律
D.反应物的总能量高于生成物的总能量时,发生放热反应
6.一定温度和压强下反应N2+3H2
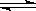 2NH3达到平衡后,下列说法正确的是( )
2NH3达到平衡后,下列说法正确的是( )
A.N2与H2不再化合,NH3不再分解
B.N2、H2化合成NH3的反应速率等于NH3分解的反应速率
C.H2、NH3的体积分数相等
D.N2、H2、NH3的物质的量浓度相等
5.下列反应中生成H2的速率最快的是 ( )
|
|
金属 |
酸溶液 |
温度 |
|
A |
Mg |
0.5mol·L━1 H2SO4 |
20℃ |
|
B |
Fe |
1 mol·L━1HCl |
20℃ |
|
C |
Mg |
2 mol·L━1HCl |
20℃ |
|
D |
Mg |
1 mol·L━1H2SO4 |
30℃ |
4.下列叙述正确的是 ( )
A.阴、阳离子之间有强烈的吸引作用而没有排斥作用,所以离子键的核间距相当小;
B.共价化合物可能含有离子键; C.离子化合物中只含有离子键 ;
D.水结成冰体积膨胀、密度变小,这一事实与水中存在氢键有关;
3.X和Y两元素的单质能化合生成XY型离子化合物,则X、Y可能位于 ( )
A.ⅠA族和ⅥA族 B.ⅡA族和ⅥA族; C.ⅡA族和ⅦA族 D.ⅥA族和ⅦA族
2.元素性质呈周期性变化的根本原因是 ( )
A.相对原子质量逐渐增大 B.核电荷数逐渐增大
C.核外电子排布呈周期性变化 D.元素的化合价呈周期性变化
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com