
题目列表(包括答案和解析)
19..同温同压下,两个等体积的干燥圆底烧瓶中分别
充满①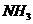 ②
②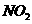 , 进行喷泉实验,如右图
, 进行喷泉实验,如右图
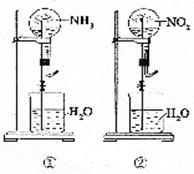
所示,经充分反应后,瓶内溶液的物质的量浓度为
A.①>② B. ①<②
C.①=② D.不能确定
答案:C
18.如图装置可以用来发生、洗涤、干燥、收集(不考虑尾气处理)气体。该装置可用于
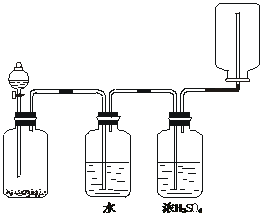
A.锌和盐酸生成氢气
 B.二氧化锰和浓盐酸生成氯气
B.二氧化锰和浓盐酸生成氯气
C.碳酸钙和盐酸生成二氧化碳
D.氯化钠和浓硫酸生成氯化氢
解析:B.需加热,C.用向上排气法收集,D.收集不到HCl。
17.在无土栽培中,要配制10 L含0.5 mol·L-1 NH4Cl、0.16 mol·L-1 KCl、0.24 mol·L-1
K2SO4的某营养液,现因无现成的KCl、K2SO4药品,而要用KCl、NH4Cl、(NH4)2SO4 三种固体配制,则需此三种固体的物质的量(mol)分别为
A.0.64、0.02、0.24 B.6.4、5.0、2.4
C.4.0、5.5、1.8 D.6.4、0.2、2.4
解析:先求出所配溶液的各种离子的物质的量:
n(NH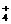 )=c(NH
)=c(NH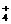 )V=0.5 mol·L-1×10 L=5
mol
)V=0.5 mol·L-1×10 L=5
mol
n(K+)=cV=[c(KCl)+2c(K2SO4)]V=(0.16 mol·L-1+2×0.24 mol·L-1)×10 L=6.4 mol
n(Cl-)=c(Cl-)V=[c(NH4Cl)+c(KCl)]V=(0.5 mol·L-1+0.16 mol·L-1)×10 L=6.6 mol
n(SO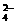 )=c(SO
)=c(SO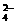 )V=0.24 mol·L-1×10 L=2.4
mol 因为K+全部由KCl提供,SO
)V=0.24 mol·L-1×10 L=2.4
mol 因为K+全部由KCl提供,SO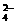 全部,由(NH4)2SO4提供,所以,n(KCl)=n(K+)=6.4
mol
全部,由(NH4)2SO4提供,所以,n(KCl)=n(K+)=6.4
mol
n((NH4)2SO4)=n(SO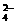 )=2.4 mol
)=2.4 mol
n(NH4Cl)=n(Cl-)-n(KCl)=6.6 mol-6.4 mol=0.2 mol 答案:D
16.下列说法正确的是
A.1 mol O2占有的体积约为22.4 L
B.22.4 L N2含阿伏加德罗常数个氮分子
C.在标准状态下,22.4 L水的质量约为18 g
D.22 g二氧化碳与标准状况下11.2 L HCl含有相同的分子数
解析:A说法错误,因为O2占有的体积除了与O2的物质的量有关外,还与O2的温度和压强有关;B说法错误,因为22.4 L N2不一定是1 mol;C说法错误,因为在标准状况下水不是气体;D说法正确,因为22 g CO2为0.5 mol,标准状况下的11.2 L HCl也是0.5 mol。 答案:D
15. 下列实验现象的描述错误的是( )。
A、新制氯水使碘化钾试纸呈蓝色
B、向NaHCO3固体加入新制氯水,有无色气体产生
C、向FeCl2溶液中滴加新制氯水,再滴加KSCN溶液,呈血红色
D、在新制氯水中滴加AgNO3溶液有白色沉淀生成
答案:A
14.在100 g 10%的盐酸和100 g 15%的盐酸中,分别加入2.3 g钠,钠全部反应后产生的气体
A.一样多
B.在浓度大的盐酸中反应产生的气体多
C.在浓度小的盐酸中反应产生的气体多
D.由反应剧烈程度决定
解析:加入的Na先与盐酸溶液中的HCl反应,然后再与H2O反应。水是足量的,加入的Na能够反应完全,所以产生的H2一样多。 答案:A
13.精确配制一定物质的量浓度的NaOH溶液,下面实验操作正确的是
A.称量时,将NaOH固体直接放在天平托盘上面的纸上
B.将称好的NaOH固体放入容量瓶中,加入少量水溶液
C.在烧杯中溶解NaOH固体后,立即将溶液注入容量瓶中
D.将烧杯中已冷却的NaOH溶液注入未经干燥的容量瓶中
解析:用固体物质配制溶液的一般步骤为:计算→称量→溶解→转移→洗涤→定容→摇匀。溶解是在烧杯中进行的,溶解后的溶液冷却后才能转移,洗涤后的溶液也应转移到容量瓶中。A.NaOH具有吸湿性和腐蚀性,不能直接放在天平托盘或在纸上称量,应放在玻璃器皿中称量,如小烧杯中;B.固体物质应在烧杯中溶解(NaOH固体溶解时放出大量热);C.NaOH溶解后,应将溶液冷却到室温,再转移到容量瓶中,否则会使结果偏大;D.未经干燥的容量瓶对浓度没有影响。 答案:D
12.硫代硫酸钠可作为脱氯剂,实验发现25.00 mL 0.100 mol·L-1 Na2S2O3溶液恰好把224 mL(标准状况)Cl2完全转化为Cl-,则S2O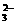 转化成了
转化成了
A.S2- B.S C.SO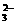 D.SO
D.SO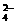
解析:设Na2S2O3中硫元素的化合价从+2升高到+x,根据化合价升降相等列式得:
2×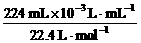 =2(x-2)×25.00 mL×10-3
L· mL-1×0.100 mol·L-1
=2(x-2)×25.00 mL×10-3
L· mL-1×0.100 mol·L-1
解得x=6 可知S2O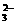 转化成了SO
转化成了SO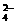 。
答案:D
。
答案:D
11. 患甲状腺肿大是边远山区常见的地方病,下列元素对该病有治疗作用的是( )
A.钠元素 B.氯元素 C.碘元素 D.铁元素
答案:C
10.有一无色溶液,可能存在于其中的离子组是
A.K+、Na+、OH-、Cl-
B.Cu2+、Ba2+、NO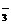 、Cl-
、Cl-
C.Na+、Mg2+、OH-、SO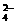 D.Ba2+、H+、NO
D.Ba2+、H+、NO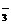 、CH3COO-
、CH3COO-
解析:A组离子无色且相互之间不反应,可能大量共存于无色的同一溶液中;B组离子中的Cu2+在水溶液中为淡蓝色;C组离子中的Mg2+与OH-能反应,不能大量存在于同一溶液中;D组离子中的H+与CH3COO-能反应,不能大量共存于同一溶液中。 答案:A
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com