
题目列表(包括答案和解析)
5.氢化钠(NaH)是生氢剂,可发生如下反应:NaH + H2O == NaOH + H2↑,对这一反应的叙述正确的是
A.NaH是氧化剂 B.NaOH是氧化产物
C.NaOH是还原产物 D.氧化产物和还原产物的质量比是1:1
4.吸进人体内的氧有2%转化为氧化性极强的活性氧,这些活性氧能加速人体衰老,被称为“生命杀手”。中国科学家尝试用Na2SeO3清除人体内活性氧,Na2SeO3的作用是
A.还原剂 B.氧化剂
C.既是氧化剂又是还原剂 D.既不是氧化剂又不是还原剂
3. 下列比较不正确的是
A.熔点:Li>Na>K B.热稳定性:Na2CO3>CaCO3>NaHCO3
C.密度:煤油<Li<Na<H2O D.还原性:Li<Na<K
2.据报道,某国一集团拟在太空建造巨大的集光装置,把太阳光变成激光用于分解海水制
|
氢气:2H2O === 2H2↑ + O2↑ 下列说法不正确的是( )
A. 水的分解反应是放热反应
B. 反应物所具有的总能量低于生成物所具有的总能量
C. 使用氢气做燃料有助于控制温室效应
D. 氢能源将是21世纪中后期最理想的能源剂
1.下列元素属于碱金属元素的是
A.Pb B.Sb C.Rb D.Lu
29(10分)某学生设计了如下实验:
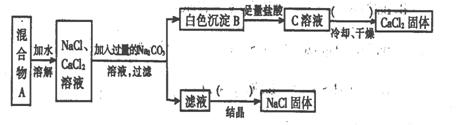
回答下列问题:
(1)该同学的实验目的是 ;
(2)上图括号内的操作步骤均为 ;
(3)按此实验方案得到的NaCl固体中肯定含有
(填化学式)杂质;为了解决这个问题可以向过滤得到的滤液中加入适量的 ;
(4)写出生成B的离子方程式:
30(6分)实验室中需要配制500mL 0.10 mol·L-1的NaOH溶液,就该实验回答下列问题。
(1)用天平称量NaOH固态 __ g。称量NaOH固体需注意以下两个问题:①因为NaOH具有腐蚀性,所以称量时,需注意选择用 盛装NaOH固体;
②称量必须迅速,目的是 。
(2)实验所需的仪器有容量瓶(规格是: )、托盘天平、烧杯、胶头滴管、,还有 。
(3)下列操作对所配制的溶液浓度肯定没有影响的是 。
A.称量时已观察到NaOH吸水
B.将烧杯中溶解后的溶液注入容量瓶,然后直接添加蒸馏水至刻度线
C.摇匀定容后,用胶头滴管向容量瓶中再滴加蒸馏水至刻度线
D.配制溶液前用蒸馏水润洗容量瓶
四 本题包括1小题,共10分
31、用KMnO4与足量浓度为12mol/L的浓盐酸反应.反应方程式如下:
2KMnO4 + 16HCl = 2KCl + 2MnCl 2+ 5Cl 2↑ + 8H2O
回答下列问题:
(1)该反应中的氧化剂是 、氧化产物是 。
(2)2molKMnO4完全反应,至少需要HCl物质的量为 mol。
(3)8mol HCl完全反应,产生的Cl 2在标准状况下的体积为多少升?
26、(5分)2006年夏天,中国南部沿海地区洪灾过后,饮用水的消毒杀菌成为抑制大规模传染性疾病爆发的有效方法之一。漂白粉是常用的消毒剂。
(1)工业上将氯气通入石灰乳[Ca(OH)2]制取漂白粉,化学反应方程式:
。
(2)漂白粉的有效成分是(填化学) 。
(3)漂白粉溶于水后,受空气中的CO2作用,即产生有漂白、杀菌作用的次氯酸,化学反应方程式为 。
27(6分)将一小块钠投入一盛有水的烧杯中,发生下列现象,请说明原因:
① 钠浮在水面上________________________;
② 钠与水剧烈反应并熔成一个闪亮的小球 ;
③小球在水面上四处游动_______________________________;
④反应后在溶液中加几滴酚酞溶液,溶液变红________________________;
⑤写出钠与水反应离子方程式
28(8分)下表是某地市场上销售的一种“加碘盐”包装上的部分文字说明。請根据此表,结合中学学过的化学知识,回答下列问题:
|
配料表 |
精制海盐、碘酸钾(KIO3) |
|
含碘量 |
20―40mg/kg |
|
储藏方法 |
密封避光、防潮 |
|
食用方法 |
烹调时待食品熟后加入碘盐 |
⑴据物质分类中的树状分类法有关知识,在:①HIO3 ②碘酸钠 ③KOH ④I2O5 ⑤HI
五种 (填“混合物”或“化合物”或“盐”或“氧化物”)中与碘酸钾(KIO3)属于同类物质的有 (填序号)。
⑵推测出碘酸钾(KIO3)的物理性质:碘酸钾(KIO3) 溶于水(填“能”或“不能”),化学性质:碘酸钾(KIO3)在受热时 。
25、下列关于碳酸钠的说法正确的是:
A 同条件下,水中溶解度小于碳酸氢钠
B 同条件下,盐酸中反应速率大于碳酸氢钠
C 热稳定性大于碳酸氢钠
D 固体中混有碳酸氢钠时可通过加热法除去杂质
第Ⅱ卷 (非选择题 共45分)
24、将少量氯水加入KI稀溶液中振荡,再加入CCl4,振荡,静置后观察到的现象是:
A 形成均匀的紫红色溶液 B 有紫色沉淀析出
C 液体分层,上层呈紫红色 D 液体分层,下层呈紫红色
23、 He 可以作为核聚变材料,下列关于
He 可以作为核聚变材料,下列关于 He的叙述正确的是
He的叙述正确的是
A.  He 和
He 和 H 互为同位素
H 互为同位素
B.  He 原子核内中子数为2
He 原子核内中子数为2
C.  He 原子核外电子数为2
He 原子核外电子数为2
D.  He 代表有2个质子和3个中子的氦原子
He 代表有2个质子和3个中子的氦原子
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com