

题目列表(包括答案和解析)
6.C解析:欲使Mg2+全部转化成沉淀并从溶液中分离出来,应向溶液中加入过量的NaOH溶液,使Mg2+、Al3+全部沉淀后,再使Al(OH)3恰好溶解。设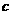 (Al3+)=
(Al3+)=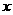 mol·L-1,则根据电荷守恒:
mol·L-1,则根据电荷守恒:
3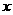 +2
+2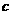 (Mg2+)
(Mg2+)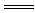
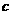 (Cl-),即3
(Cl-),即3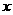 +2×0.2=1.3,
+2×0.2=1.3,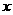 =0.3mol·L-1。
=0.3mol·L-1。
设NaOH溶液的体积为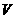 mL,
mL,
则根据关系式:Mg2+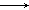 2OH-
2OH-
5.D解析:因为Al(OH)3溶于强酸、强碱,而不溶于弱碱,所以选D。
4.D解析:由题给条件,可知将甲蒸发掉一半水分,溶质的量并未发生变化,故完全反应时消耗的盐酸应与丙相同,甲丙很容易判断。由于存在如下关系式:2NaOH-Na2CO3-2HCl,可知向乙中通入量CO2后部分NaOH变为Na2CO3,而生成的Na2CO3在与盐酸反应时会消耗与NaOH变质前等量的盐酸,故完全反应后,所需盐酸溶液的体积应是相等的,即甲=乙=丙。
3.C解析:0.8gNaOH若全部转化成Na2CO3,则其质量为1.06g<1.37g;若全转化成NaHCO3,则其质量应为1.68g>1.37g。故NaOH吸收CO2时实际上生成了Na2CO3(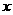 mol)和NaHCO3(
mol)和NaHCO3(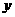 mol)的混合物。依Na原子守恒,得2
mol)的混合物。依Na原子守恒,得2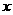 +
+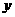 =0.02,且有:106
=0.02,且有:106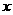 +84
+84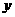 =1.37,解得
=1.37,解得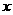 =0.005mol,
=0.005mol,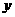 =0.01mol,故通人CO2的物质量为
=0.01mol,故通人CO2的物质量为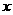 +
+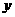 =0.015mol,质量为0.015mol×44g·mol-1=0.66g。
=0.015mol,质量为0.015mol×44g·mol-1=0.66g。
2.D 解析:A中能产生气体且能使澄清石灰水变浑浊的是NaHCO3;B中有白色沉淀生成的是Na2CO3;C中反应速度快(剧烈)的是NaHCO3;D中两者均可与Ca(OH)2反应产生白色沉淀,故无法用于鉴别。
1.D解析:NaHCO3与石灰水反应时,反应物的量不同,产物也不相同,但不管以何种比例混合,都有CaCO3生成。当加入少量石灰水时,反应方程式为:2NaHCO3+Ca(OH)2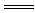 Na2CO3+CaCO3↓+2H2O;当加入过量的石灰水时,反应方程式为:NaHCO3+Ca(OH)2
Na2CO3+CaCO3↓+2H2O;当加入过量的石灰水时,反应方程式为:NaHCO3+Ca(OH)2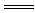 NaOH+CaCO3↓+H2O。故C正确。物质的量相等的Na2CO3和NaHCO3分别与足量盐酸反应可得等量的CO2,故D不正确。
NaOH+CaCO3↓+H2O。故C正确。物质的量相等的Na2CO3和NaHCO3分别与足量盐酸反应可得等量的CO2,故D不正确。
14.在氯化铁和氯化铜的混合溶液中,加入过量的Fe粉,若充分反应后溶液的质量没有改变,则原混合溶液中Fe3+和Cu2+物质的量之比为多少?
答案及详解:
13.用下面两种方法可以制得白色的Fe(OH)2沉淀。
方法一:用不含Fe3+的FeSO4溶液与用不含O2的蒸溜水配制的NaOH溶液反应制备。
(1)用硫酸亚铁晶体配制上述FeSO4溶液时还需加入________。
(2)除去蒸馏水中溶解的O2常采用________的方法。
(3)生成白色Fe(OH)2沉淀的操作是用长滴管吸取不含O2的NaOH溶液,插入FeSO4溶液液面下,再挤出NaOH溶液。这样操作的理由是_______。
方法二:在如图3-2装置中,用NaOH溶液、铁屑、稀NaSO4等试剂制备。
(1)在试管I里加入的试剂是________。
(2)在试管Ⅱ里加入的试剂是________。
(3)为了制得白色Fe(OH)2沉淀,在试管工和Ⅱ中加入试剂,打开止水夹,塞紧塞子后的实验步骤是________。
(4)这样生成的Fe(OH)2沉淀能较长时间保持白色,其理由是_____________________。
12.往一金属易拉罐内(内空)放入一满角匙的某白色晶体,摇动几下后,立即注入50mL6mol·L-1氢氧化钠溶液,用胶布密封罐口。过一段时间后,罐壁变瘪;再过一段时间后,瘪了的罐壁又重新鼓起。
(1)要产生上述实验现象,做易拉罐的金属是______;往罐内加入的白色晶体是______;
(2)罐壁变瘪的原因是______,反应方程式是______;
(3)罐再度鼓起的原因是______,反应方程式是______。
11.在含有1molFeSO4的溶液中投入一小块金属钠,反应完全后,滤出沉淀并洗涤之,然后在空气中灼烧沉淀得到的固体物质是( )
A.Fe B.FeO C.Fe(OH)3 D.Fe2O3
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com