

题目列表(包括答案和解析)
16.SiO2+2NaOH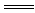 Na2SiO3+H2O
Na2SiO3+H2O
Na2SiO3+2HCl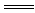 2NaCl+H2SiO3↓
2NaCl+H2SiO3↓
或Na2SiO3+CO2+H2O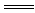 Na2CO3+H2SiO3↓
Na2CO3+H2SiO3↓
Na2SiO3+2CO2+2H2O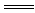 2NaHCO3+H2SiO3↓
2NaHCO3+H2SiO3↓
解析:SiO2难溶于水,不能与水发生反应,这样就只能先用SiO2与其他物质先作用生成硅酸盐,再根据硅酸是弱酸,用硅酸盐与酸作用来制备硅酸。
点评:一般来说,受热易分解的酸或碱,其对应的氧化物则不能与水反应,如H2SiO3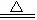 H2O+SiO2,则SiO2不能与水反应;Cu(OH)2
H2O+SiO2,则SiO2不能与水反应;Cu(OH)2 CuO+H2O,则CuO不能与水反应。硅酸不能溶于水,且不能溶于(HCl、H2SO4、HNO3等)强酸。不溶于强酸的物质还有:CuS、Ag2S、PbS、HgS、AgCl、AgBr、AgI、BaSO4等。
CuO+H2O,则CuO不能与水反应。硅酸不能溶于水,且不能溶于(HCl、H2SO4、HNO3等)强酸。不溶于强酸的物质还有:CuS、Ag2S、PbS、HgS、AgCl、AgBr、AgI、BaSO4等。
15.不矛盾;原因见上。
解析:本题利用CO2、SiO2、Na2SiO3、H2CO3、H2SiO3等化合物的性质,考查同学们的逻辑推理能力以及思维的敏捷性和深刻性。反应①是在溶液中进行的反应,反应之所以能够发生,是由于酸性H2CO3>H2SiO3,反应符合“强酸制弱酸”的复分解反应原理;而反应②是在高温熔融状态下的反应,由于CO2可从熔融体中逸出,使得反应可以发生,而与酸性H2CO3>H2SiO3无关。
点评:①是在水溶液中进行的复分解反应,②是固体与固体之间的反应(非水条件);①是常温下的反应,②是高温条件下的反应。两个反应的条件不同,实质上没有可比性,因为它们的反应原理、反应条件与本质均不同。
14.Na2SiO3 Si SiO2 CaSiO3
13.SiO2 Na2SiO3 CO2 H4SiO4 H2SiO3
12.2NaOH+SiO2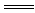 Na2SiO3+H2O
Na2SiO3+H2O
11.D解析:SiO2不溶于除氢氟酸以外的酸,CaO、CaCO3均可溶于盐酸且CaCO3溶于盐酸有气泡生成,SiO2可以溶于NaOH溶液。本题应选D。
10.D解析:硅的非金属性比碳弱,A项错;硅在地壳中的含量在所有的元素中居第二位,排名前四位的是O、Si、Al、Fe,所以B项错;硅在自然界中是以化合态存在的,所以C项也错,答案应选D。
9.C解析:SiO2是酸酐的原因应当是它与强碱溶液反应只生成盐和水,它不溶于水,对应的酸H2SiO3也不是强酸,故应选C。
8.D 解析:Ca(HCO3)2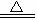
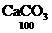 +
+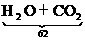 ↑①
↑①
CaCO3 CaO+CO2↑②
CaO+CO2↑②
由①可知当Ca(HCO3)2全部分解后,剩余固体质量大于一半,所以只有②也发生反应才有可能使质量减少一半。又因为Ca(HCO3)2稍加热就分解,而CaCO3必须在高温下才分解。即当CaCO3发生分解时,Ca(HCO3)2已全部分解完毕。
7.BD解析:酸酐与对应的酸中心元素化合价相同,SiO2和H2SiO3的化合价相同,所以SiO2尽管难溶于水,但它仍是硅酸的酸酐,A正确;SiO2为原子晶体,故SiO2不能表示其分子组成,即二氧化硅中并不存在SiO2分子,B错误;二氧化硅难溶于水,且不与水反应,无法直接与水反应制取硅酸,C正确;SiO2与HF酸反应的方程式为:SiO2+4HF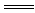 SiF4↑十2H2O,SiF4不是盐,SiO2与HF酸反应只是一种特殊情况,所以不能说SiO2是两性氧化物,D错误。
SiF4↑十2H2O,SiF4不是盐,SiO2与HF酸反应只是一种特殊情况,所以不能说SiO2是两性氧化物,D错误。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com