
题目列表(包括答案和解析)
5.实验室保存下列物质的方法中,不正确的是( )
A.少量金属钠保存在煤油里
B.澄清石灰水盛装在用玻璃塞塞紧的试剂瓶中
C.FeSO4溶液存放在加有少量铁粉的试剂瓶中
D.新制氯水通常保存在棕色试剂瓶中
4.下列各组物质中,使有色物质褪色的反应机理相同的是( )
A.二氧化硫和过氧化钠 B.过氧化氢和次氯酸
C.二氧化硫和漂白粉 D.活性炭和二氧化硫
3.下列有关项目的比较中,错误的是( )
A.酸性:H2SiO3>H2CO3 B.氧化性:Fe3+>Fe2+
C.热稳定性:Na2CO3>NaHCO3 D.硬度:金刚石 > 刚玉
2.下列说法正确的是( )
A.Cl-和Cl2都是氯元素 B.Cl2有毒,Cl-也有毒
C.次氯酸中氯元素的化合价为+1 D.Cl2和Cl原子都呈黄色
1.下列表述正确的是( )
①开发使用新型清洁能源,减少化石燃料的燃烧,可从根本上防止酸雨的产生 ②我国从2000年起逐渐用二氧化氯取代氯气对饮用水进行消毒,因为二氧化氯杀菌、消毒能力强,持效长 ③氧化镁可用来制造耐火砖和坩埚等④明矾能使水中的悬浮物凝聚,可做为净水剂 ⑤建设三峡大坝使用了大量水泥,水泥是硅酸盐材料 ⑥给机动车安装尾气净化器,可减少光化学烟雾的发生( )
A.①④⑤ B.①②④⑤ C.②③④⑥ D.全部
19,(1)放出大量的热; 2Na2O2+2H2O = 4NaOH+O2↑
(2)打开阀门向试管中滴入少量的水,用带火星的木条,靠近a处,如果木条复燃,则有氧气生成,反之无氧气生成; 水中有气泡生成。
20,(1)BaCO3
(2)NaHCO3,BaCl2; KCl; 焰色
21,(1)钠 HCl
(2) NaOH+NH4Cl NaCl+NH3↑+H2O
NaCl+NH3↑+H2O
(3) 盐酸小液滴
22,(1)Cl2 FeCl2
(2) 4Fe(OH)2+2H2O+O2 = 4Fe(OH)3
(3) 2Fe3++Fe = 3Fe2+
23,
23﹒(9分)现有Na2CO3和NaHCO3的混合物共14.0g,现把混合物充分加热到不再有气体放出为止,发现混合物质量变为10.9g,试计算原混合物中Na2CO3的物质的量。
答案:一、1 ACACD 6 BBBBD 11 ADCAA 16 CD
20﹒(7分)有一包白色粉末可能由K2SO4、NaHCO3、BaCl2、FeCl3、KCl、NH4NO3六种物质中的某几种组成,现进行如下实验:
(1)将白色粉末加水溶解,得无色溶液。
(2)向(1)中所得的无色溶液中加入NaOH溶液并加热,仅观察到有白色沉淀A生成,过滤后,向滤液中滴加硝酸酸化的AgNO3溶液,又得到白色沉淀B。
根据上述现象判断:
(1)白色沉淀A的化学式是 。
(2)原白色粉末中一定含有 ,可能含有 ,对可能含有的物质,可通过 反应进一步检验。
21﹒(7分)已知A是一种金属,B溶液能使酚酞试液变红,且焰色反应呈黄色;D、F相遇会产生白烟。A、B、C、D、E、F间有如下变化关系:
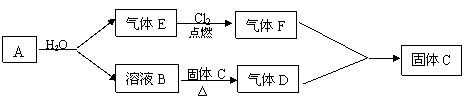
(1)A的名称是 ;F的化学式是 。
(2)B→D反应的化学方程式为 。
(3)F在空气中遇水蒸气产生白雾现象,这白雾实际上是 。
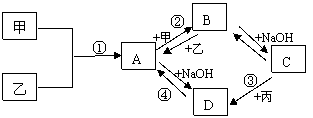 22﹒(8分)已知:甲、乙、丙为常见单质,甲常温下为固体,乙为一黄绿色气体,丙为无色气体。A、B、C、D均为化合物,D为一红褐色沉淀,它们之间有下图转化关系。请回答以下问题。
22﹒(8分)已知:甲、乙、丙为常见单质,甲常温下为固体,乙为一黄绿色气体,丙为无色气体。A、B、C、D均为化合物,D为一红褐色沉淀,它们之间有下图转化关系。请回答以下问题。
(1)写出下列物质的化学式;乙 ;B 。
(2)写出③反应的化学方程式: 。
(2)写出②反应的离子方程式: 。
18﹒(10分)某同学要配制1.0 mol/L的NaOH溶液,提供的仪器有①容量瓶(250mL)②玻璃棒 ③托盘天平(配砝码和镊子) ④药匙 ⑤胶头滴管 ⑥烧杯 ⑦漏斗
(1)上述仪器中配制溶液时所需的玻璃仪器有 (填序号),容量瓶上标有①温度 ②浓度 ③容量 ④压强 ⑤刻度线 ⑥酸式或碱式六项中
(填序号)。
(2)用托盘天平和小烧杯称取NaOH时,有下列操作步骤,正确的顺序是
(有的操作可重复使用)
A﹒调整天平零点
B﹒将砝码放回砝码盒中,将游码拨回零刻度
C﹒称取小烧杯的质量
D﹒称取小烧杯和NaOH的质量
E﹒记录称量的数据
(3)由题意可知,你应该称取固体NaOH g,如果由于称量时间过长,你所配制的NaOH溶液的浓度与要求相比 (填“偏大”“偏小”“相等”) 。
19﹒(8分) 用脱脂棉包住0.2g过氧化钠粉末,置于石棉网上,往脱脂棉上滴几滴水,可观察到脱脂棉剧烈燃烧起来。
(1)由上述实验现象可得出两条有关过氧化钠跟水反应的结论是:
第一:有氧气生成;第二: 。
(2)某研究性学习小组拟用如下图所示的装置进行实验,以验证上述结论。
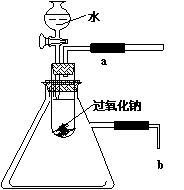 用以验证第一条结论的实验操作是
用以验证第一条结论的实验操作是
,
现象是 。
为了验证第二条结论,将管口b浸入水中,可观察
到的现象为
。
1﹒孔林、孔庙、孔府是著名的旅游景点,近几年,修建的高速公路绕开了孔林、孔庙、孔府,以减少污染。你认为,在三孔景区,这样能有效减少的主要是
A﹒车辆排放的大气尾气 B﹒居民燃煤所产生SO2气体
C﹒车辆尘埃、生活垃圾 D﹒工厂所排“三废”
2﹒下列每组分别给出了两个量,其中可以组成一个物质的量的公式的组有
|
① |
② |
③ |
④ |
⑤ |
|
物质微粒数 |
固体体积 |
溶液的质量百分比浓度 |
标准状况下气体的摩尔体积 |
非标准状况下某物质的质量 |
|
阿伏加德罗常数 |
固体密度 |
溶液体积 |
标准状况下气体的体积 |
物质的摩尔质量 |
A﹒①②⑤ B﹒②③④ C﹒①④⑤ D﹒①③④
3﹒物质分类的依据通常是根据它的组成和性质,下列物质的分类中,只考虑组成的是
A﹒硫酸钠是钠盐、硫酸盐、正盐
B﹒二氧化硫是氧化物、酸酐、有漂白性物质
C﹒氢氧化钠是一元碱、易溶性碱、强碱
D﹒碳酸氢钠是钠盐、酸式盐、易分解的盐
4﹒“纳米材料”是粒子直径为1nm-100nm的材料,纳米碳就是其中的一种。某研究所将纳米碳均匀的分散到蒸馏水中,得到的物质①是溶液 ②是胶体 ③具有丁达尔现象 ④不能透过半透膜 ⑤不能透过滤纸 ⑥静止后会出现黑色沉淀。其中正确的是
A﹒①④⑥ B﹒②③⑤ C﹒②③④ D﹒①③④⑥
5﹒下列离子方程式改写成化学方程式正确的是
A﹒Cu2+ + 2OH- = Cu(OH)2↓
CuCO3 + 2NaOH = Cu(OH)2↓ + Na2CO3
B﹒CO32- + 2H+ = CO2↑ + H2O
BaCO3 + 2HCl = BaCl2 +CO2↑ + H2O
C﹒Fe+ 2H+ = H2↑ +Fe2+
Fe+ 2HNO3 = H2↑ +Fe(NO3)2
D﹒H+ + OH- = H2O
2KOH + H2SO4 = K2SO4 + 2H2O
6﹒对四种无色溶液进行离子检验,实验结果如下,其中明显错误的是
A﹒K+ 、Na+、Cl-、NO3- B﹒Cu2+、NO3-、OH-、HCO3-
C﹒Na+、OH-、Cl-、NO3- D﹒K+ 、 Na+、 S2-、 Cl-
7﹒下列反应中,CO2作氧化剂的是
A﹒Ca(OH)2+ CO2 = CaCO3↓ + H2O
B﹒CO2 + C  2CO
2CO
C﹒2Fe2O3 +
3C  4Fe +3CO2↑
4Fe +3CO2↑
D﹒C+ 2H2O  2H2+ CO2
2H2+ CO2
8﹒地壳中含量第一和第二的两种元素所形成的化合物不具有的性质是
A﹒熔点很高 B﹒与水反应生成对应的酸
C﹒可与烧碱反应生成盐 D﹒坚硬
9﹒铜粉加入稀盐酸中,加热无现象,这时加入一种盐则铜粉溶解而溶液变蓝,同时有气体放出,这种盐是
A﹒NaCl B﹒KNO3 C﹒FeCl2 D﹒Fe2(SO4)3
10﹒固体甲与盐酸反应得到溶液乙,乙与氢氧化钠溶液反应生成沉淀丙,一段时间后,将丙加热又得到甲,则甲可能是
A﹒Fe B﹒Al C﹒FeO D﹒CuO
11﹒某溶液中,滴加KSCN溶液时无明显现象发生,再滴入少量氯水,溶液立即显红色。则原溶液中一定含有的是
A﹒Fe2+ B﹒Fe3+ C﹒K+ D﹒NH4+
12﹒用坩埚钳夹住一小块刚用盐酸处理过的铝箔,在酒精灯上加热至熔化,发现熔化的铝箔不滴落。下列关于上述实验中有关问题的解释不正确的是
A﹒铝箔熔化,失去金属光泽 B﹒铝在空气中能很快形成氧化膜
C﹒氧化铝的熔点比铝高 D﹒氧化铝与盐酸不反应
13﹒将预先称量的20g蔗糖放入100mL烧杯中,加几滴水搅拌均匀,再加入15mL浓硫酸,用玻璃棒迅速搅拌,观察到蔗糖由白变黑,体积膨胀,呈疏松海绵状,有刺激性气味气体生成,放出大量的热,在此过程中浓硫酸没表现出的化学性质是
A﹒吸水性 B﹒脱水性 C﹒酸性 D﹒氧化性
14﹒关于硝酸的说法正确的是
A﹒硝酸与金属反应时,主要是+5价的氮得电子
B﹒浓硝酸与浓盐酸按3︰1的体积比所配成的溶液叫王水
C﹒硝酸电离出的氢离子,内被Zn、Fe等金属还原成H2
D﹒常温下,向浓硝酸中投入Fe片,会产生大量的红棕色气体
15﹒下列选项的括号内是除去杂质所用的试剂,其中错误的是
A﹒二氧化氮中混有NO(水)
B﹒NaNO3溶液中混有Na2SO4(Ba(NO3)2)
C﹒氯气中混有水蒸气(浓硫酸)
D﹒氨气中混有水蒸气(NaOH固体)
16﹒下列两种物质中所含分子数目相同的是
A﹒2g氢气和8g氦气
B﹒常温常压下,2L氢气和2L水
C﹒常温常压下1mol氧气和标准状况下32g氧气
D﹒常温常压下,22.4L氧气和2g氢气
17﹒现有两种气体,SO2和Cl2,下列方法或试剂(必要时可加热)能用于鉴别它们的是:①观察颜色 ②石蕊试剂 ③品红溶液
A﹒只有①② B﹒只有①③ C﹒只有②③ D﹒①②③
第II卷(非选择题 共49分)
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com