
题目列表(包括答案和解析)
19、(9分)
(1)含分子数最多的是(填序号,下同)__ __ __, 含原子数最少的是___ ____,质量最大的是____ ___,体积最小的是_ ______。
⑵写出过氧化钠和水反应的化学方程式 _____
氧化剂是 ,还原剂是 ,转移电子个数为_ ____________。
2、所得溶液溶质的质量分数?
高一化学第一学期期中试卷
|
|
|
|
|
题 |
|
名 姓 |
答 |
|
|
准 |
|
号 学 |
不 |
|
|
内 线 |
|
级 班 |
封 |
|
|
密 |
|
校 学 |
|
|
|
|
高一化学期中试卷答卷纸
26、(9分)有一表面被氧化成氧化钠的金属钠样品5.22g,投入到100g水中,产生气体2.24L(标况)。
求:1、此样品中单质钠的物质的量?
25、(4分)将浓度为a%的NaOH溶液蒸发掉mg水后,变成2a%的NaOH不饱和溶液VmL。求所得NaOH溶液的物质的量浓度。
24、(6分)对于混合物的分离或提纯,常采用的方法有:过滤、蒸发、蒸馏、萃取、洗气、加热分解等。下列各组混和物的分离或提纯应采用什么方法?
①实验室中的石灰水久置,液面上常悬浮有CaCO3微粒。可用 的方法除去Ca(OH)2溶液中悬浮的CaCO3微粒。
②除去H2中的CO2,可用 的方法除去。
③除去乙醇中溶解的微量食盐可采用 的方法。
④粗盐中含有不溶性的泥沙、可溶性的氯化钙、氯化镁及一些硫酸盐。要将粗盐提纯,可先将粗盐溶解,按一定的顺序加入沉淀剂,再 ;然后将溶液调成中性并
就可以得到较为纯净的氯化钠。
⑤除去氧化钙中的碳酸钙可用 的方法。
23、(7分)有一包粉末,其中可能含有Na2CO3、NaCl、K2SO4、FeCl3、BaCl2、K2CO3和Na2SO4,现按下列步骤进行实验:
(1)将该粉末溶于水得无色溶液和白色沉淀
(2)在滤出的沉淀中加入足量稀HNO3后,有部分沉淀溶解,同时产生无色气体
(3)取滤液做焰色反应,火焰呈黄色,隔着蓝色钴玻璃观察,未见紫色火焰。
(提示:钠的焰色反应火焰呈黄色,钾的焰色反应隔着蓝色钴玻璃观察,有紫色火焰)
由上述实验现象推断:混合物中一定含有 ,一定不含有 ,不能肯定是否含有 。
22、(7分)实验室配制500mL、0.2mol/L的Na2SO4溶液,实验操作步骤有:
A.在天平上称出14.2g硫酸钠固体,把它放在烧杯中,用适量的蒸馏水使它完全溶解并冷却至室温。B.把制得的溶液小心地转移至容量瓶中。C.继续向容量瓶中加蒸馏水至液面距刻度1cm~2cm处,改用胶头滴管小心滴加蒸馏水至溶液凹面底部与刻度线相切。D.用少量蒸馏水洗烧杯和玻璃棒2-3次,每次洗涤的液体都小心注入容量瓶,并轻轻振荡。E.将容量瓶塞塞紧,充分摇匀。请填写下列空白:
(1)操作步骤的正确顺序为(填序号) 。
 (2)本实验用到的基本仪器已有烧杯、天平(砝码、镊子)、玻璃棒,还缺少的仪器是
、
、
。
(2)本实验用到的基本仪器已有烧杯、天平(砝码、镊子)、玻璃棒,还缺少的仪器是
、
、
。
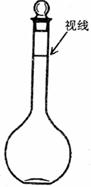
(3)下列情况会使所配溶液浓度偏高的是(填序号)
a.某同学观察液面的情况如图所示
b.没有进行上述的操作步骤D
c.加蒸馏水时,不慎超过了刻度线
d.砝码上沾有杂质
e.容量瓶用前内壁沾有水珠
21、(9分)某实验小组对中学课本中可生成氢气的反应进行了研究,总结出三个可以生成H2的反应:①Zn+盐酸 ②Na+水 ③Al+NaOH溶液。为点燃上述三个反应生成的H2,他们设计了如下装置图:
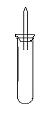 请回答下列问题:
请回答下列问题:
⑴写出Na与H2O反应的离子方程式 ;
⑵在点燃H2之前必须先进行 ,方法是
;
⑶实验小组在点燃用上述装置制得的H2时,①③实验获得成功,②却
失败了。他们分析认为失败的原因是Na与H2O的反应速率太快,Na的
用量太少。于是他们准备增加钠的用量,可老师说太危险,你认为产生危
险的原因是 。
⑷实验小组查阅钠、苯、水的密度分别为0.97g/mL、0.88g/mL、1.00g/mL,并据此对实验进行了改进。



原实验 改进后实验
在改进后的实验中H2的生成速率减慢。原因是
。
20、(3分)已知高锰酸钾和氢溴酸发生反应:2KMnO4+16HBr=2KBr+2MnBr2+5Br2↑+8H2O
(1)反应中的还原剂_________________;
(2)若消耗15.8 g氧化剂,则被氧化的还原剂的物质的量是__________mol。
19、(9分)⑴在标准状况下,物质①4gH2,②33.6LCH4,③1molH2O,④3.01×1023个O2.含分子数最多的是(填序号,下同)__ __ __,含原子数最少的是___ ____,质量最大的是____ ___,体积最小的是_ ______。
⑵写出过氧化钠和水反应的化学方程式 ______
在此反应中,氧化剂是 ,还原剂是 ,每有1mol过氧化钠反应,则转移电子个数为_____________。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com