
题目列表(包括答案和解析)
21、(7分)某无色透明的澄清溶液,可能含有较大量的Cu2+、OH-、NO3-、Cl-、
HCO3-、H+、K+等离子中的两种或多种,现进行如下实验:
①取溶液少量加入碳酸钠粉末有无色无味气体放出;
②另取原溶液少许,加入硝酸银溶液无沉淀生成。
(1)由此判断原溶液中一定含有的离子是 ;一定不含有的离子是
;可能含有的离子是 。(1分/空)
(2)为了检验上述溶液中可能含有的离子是否一定存在,你认为还应该继续进行
的实验操作是: ;对应的实验现象
和结论是 。(2分/空)
20、(12分)X、Y、Z和W代表原子序数依次增大的四种短周期非金属元素,它们满足以下条件:①元素周期表中,Z与Y相邻,Z与W相邻;X无中子。
②Y、Z和W三种元素的原子最外层电子数之和为17。
请填空:
(1)Y、Z和W三种元素是否位于同一周期(填“是”或“否”):____,
理由是 。
(2)Y是________,Z是__________,W是__________。(用化学符号填空)
(3)X、Y、Z和W可组成一化合物,其原子个数之比为8:2:4:1,
写出该化合物的化学式_____________。(2分/空)
19、(8分)在原子序数1-18号元素中:(用化学符号填空)
(1)与水反应最剧烈的金属是_____________。
(2)与水反应最剧烈的非金属单质是_____________。
(3)在室温下有颜色的气体单质是_____________。
(4)除稀有气体外,原子半径最大的元素是_________。
(5)原子半径最小的元素是_____________。
(6)气态氢化物水溶液呈碱性的元素是_____________。
(7)气态氢化物最稳定的化学式是_____________。
(8)最高价氧化物对应水化物的酸性最强的元素是_____________。(1分/空)
18、向20ml1mol/L NaHCO3溶液中通入一定量的SO2后恰好完全反应,在生成的溶液中Na+和溶液中化合态硫的物质的量之比为4:3,则通入的SO2在标准状况下的体积为
A 0.448L B 0.336L C 0.224L D 0.112L
第II卷(共46分)
二:填空题
17、密度为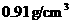 的氨水,其溶质的质量分数为0.25,该氨水用等体积的水稀释后,所得氨水的质量分数为( )
的氨水,其溶质的质量分数为0.25,该氨水用等体积的水稀释后,所得氨水的质量分数为( )
A.等于12.5% B.大于12.5%
C.小于12.5% D.无法确定
16、在野外,为了迅速得到氢气,可以用较纯的硅粉与干燥的氢氧化钙和氢氧化钠混合,加强热,即可迅速得到氢气,反应方程式Si+Ca(OH)2+2NaOH=Na2SiO3+CaO+2H2 ,在这个反应中,Si的作用是
,在这个反应中,Si的作用是
A.还原剂 B.氧化剂 C.催化剂 D.既是氧化剂又是还原剂
15、能够说明硫的非金属性比氯弱的事实有:
①Cl2与铁反应生成FeCl3,S与铁反应生成FeS;
②Cl2和H2的混合气,经强光照射可剧烈反应,而S与H2反应需较高温度;
③将Cl2通入氢硫酸中可置换出硫;
④常温时硫单质为固态而氯单质为气态。
A.①③ B.①②③ C.②④ D.①②③④
14、标准状况下将一充满NO2 NO O2混合气体试管倒立于水中,气体全溶解且无气体剩余,若试管内的产物不扩散,则试管内溶液的物质的量浓度为.
A. 1/39.2<C<1/28 B. 0<C<1/22.4
C. 1/39.2<C<1/22.4 D. 1/28<C<1/22.4
13、将木炭与浓H2SO4共热后得到的气体通入下列溶液中,溶液不可能出现浑浊的是
A.泡花碱 B.饱和H2S溶液 C.足量Ba(OH)2溶液 D.溴水
12、下列离子方程式书写正确的是
A. 过量的NaHSO4和Ba(OH)2溶液反应:
H+ + SO42- + Ba2+ + OH -= BaSO4↓+ H2O
B. NH4HCO3和过量NaOH溶液相混合: HCO3- + OH- = CO32- + H2O
C. FeS和稀H2SO4反应: FeS + 2H+ == H2S↑+ Fe2+
D. 用氨水吸收少量SO2: NH3 + H2O + SO2 = NH4+ + HSO3-
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com