
题目列表(包括答案和解析)
35.(4分)加热10.0克碳酸钠和碳酸氢钠的混合物至质量不再变化,剩余固体的质量为8.45克,求混合物中碳酸钠的质量分数。
34.(4分)某种待测浓度的H2SO4溶液20mL,加入10mL0.5mol·L-1 BaCl2溶液,恰好完全反应。问(1)得到BaSO4沉淀多少克?(2)待测H2SO4溶液的物质的量浓度是多少?
33.(10分) 在常温下,Fe与水并不起反应,但在高温下,Fe与水蒸气可发生反应。 应用下列装置,在硬质玻璃管中放入还原铁粉和石棉绒的混合物,加热,并通入水蒸气,就可以完成高温下“Fe与水蒸气的反应实验”。
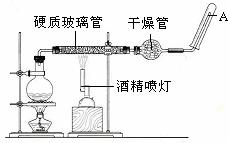
请回答该实验中的问题。
(1)写出该反应的反应方程式: ;该氧化还原反应的氧化剂是 ,转移电子数为 。
(2)实验前必须对整套装置进行 。
(3)圆底烧瓶中盛装的水,该装置受热后的主要作用是 ;烧瓶底部放置了几片碎瓷片,碎瓷片的作用是 。
(4)干燥管中盛装是的物质是 ,作用是 。
(5)试管中收集气体是 ,如果要在A处玻璃管处点燃该气体,则必须对该气体进行 。
32.(4分)用Na2CO3固体配制1mol·L-1 的Na2CO3溶液100mL。
(1)供选用的仪器有:①玻璃棒;②胶头滴管;③100mL量筒;④100mL容量瓶;⑤250mL量筒;⑥天平;⑦50mL烧杯;应选用的仪器(填编号) 。
(2)应称取Na2CO3的质量为 。
31.已知有以下物质相互转化,其中A为单质。
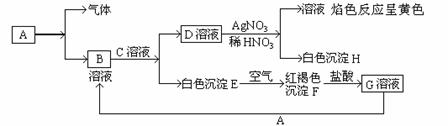
试回答:(1)写出B的化学式 D的化学式 。
(2)写出由A生成B的离子方程式 。
(3)写出由E转变成F的化学方程式 。
(4)向G溶液加入A的有关离子反应方程式 。
30.(6分)火药是中国的“四大发明”之一,永远值得炎黄子孙骄傲,也永远会激励着我们去奋发图强。黑火药在发生爆炸时,发生如下的反应:2KNO3+3C+S===K2S+N2↑+3CO2↑。其中被还原的元素是 ,被氧化的元素是 ,氧化剂是 ,还原剂是 ,氧化产物是 ,还原产物是 。
29.(6分)(1)鉴别KCl溶液和K2CO3溶液的试剂是 ,
有关离子方程式为 。
(2)除去混入NaCl溶液中少量NaHCO3杂质的试剂是 ,
有关离子方程式为 。
(3)除去Na2CO3粉末中混入的NaHCO3杂质用 方法,
有关化学方程式为 。
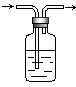
28.化学实验中的很多气体是用盐酸来制取的,这就导致了这些制取的气体中往往含有HCl杂质,要除去HCl杂质而得到纯净的目标气体,可用右图所示装置。如果广口瓶中盛装的是饱和NaHCO3溶液,则装置可以用于下列哪种气体除杂质
A.H2 B. O2 C. N2 D.CO2
以下试题答案请写在答题纸上。
27.根据反应(1)-(4),可以判断下列4个物质的氧化性由强到弱的正确顺序是
(1)Cl2+2KI=2KCl+I2 (2)2FeCl2+Cl2=2FeCl3
(3)2FeCl3+2HI=2FeCl2+2HCl+I2 (4)H2S+I2=S+2HI
A.H2S>I2>Fe3+>Cl2 B.Cl2>Fe3+>I2>H2S
 C.Fe3+>Cl2>H2S>I2. D.Cl2>I2>Fe3+>H2S
C.Fe3+>Cl2>H2S>I2. D.Cl2>I2>Fe3+>H2S
26.下列各组物质相互之间发生反应后,再向得到的溶液中滴入KSCN溶液,溶液变成红色的是
A.氯水和FeCl2溶液 B.铁屑和CuCl2溶液
C.铁屑和过量的稀硫酸 D.过量的铁屑和FeCl3溶液
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com