
题目列表(包括答案和解析)
25、某种由K 2 S和Al 2 S 3 组成的混合物中,这两种组分的物质的量之比为3∶2 ,那么
含有32 g 硫元素的该混合物的质量是( )
A. 35 g B. 50 g C. 60 g D. 70 g
24、 镁、锂在元素周期表中具有特殊的“对角线”位置关系,它们的性质相似,例如,它
们的单质在过量氧气中燃烧时均只能生成正常的氧化物 …… 等。以下叙述锂的性质正确的是( )
A. Li2SO4难溶于水 B. Li与水剧烈反应
C. LiOH是易溶于水,受热不分解的强碱 D. Li2CO3受热分解,生成Li2O和CO2
23、V mL Al2(SO4)3溶液中含有Al3+a g,取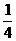 V mL溶液稀释到4V mL,则稀释后溶液中的SO42-的物质的量浓度是( )
V mL溶液稀释到4V mL,则稀释后溶液中的SO42-的物质的量浓度是( )
A.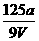 mol/L B.
mol/L B.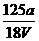 mol/L
C.
mol/L
C.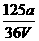 mol/L D.
mol/L D.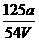 mol/L
mol/L
22、 将2mol SO2和1mol O2充入一容积固定的密闭容器中,在一定条件下反应:2SO2(g)+
O2(g) 2SO3(g),下列哪些情况能说明化学反应已达平衡状态的是( )
将2mol SO2和1mol O2充入一容积固定的密闭容器中,在一定条件下反应:2SO2(g)+
O2(g) 2SO3(g),下列哪些情况能说明化学反应已达平衡状态的是( )
A.单位时间内生成2mol SO2,同时消耗2mol SO3 B.混合气体的密度不再变化
C.单位时间内生成2mol SO3,同时消耗1mol SO2 D.混合气体的压强不再变化
21、下列反应的离子方程式书写正确的是( )
A.铁和稀盐酸反应 2Fe+6H+ 2Fe3++3H2↑
B.CO2通入足量澄清石灰水 CO2+2OH- H2O+CO32-
|
D.电解饱和食盐水 2Cl-+2H2O Cl2+H2+2OH-
20、现有如下各说法:
①在水中氢、氧原子间均以化学键相结合。
②金属和非金属化合形成离子键。
③离子键是阳离子、阴离子的相互吸引。
④根据电离方程式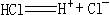 ,判断HCl分子里存在离子键。
,判断HCl分子里存在离子键。
⑤H2分子和Cl2分子的反应过程是H2、Cl2分子里共价键发生断裂生成H、Cl原子,而后H、Cl原子形成离子键的过程。
上述各种说法正确是( )
A.①②⑤正确 B.都不正确 C.④正确,其他不正确 D.仅①不正确
19、下列物质的性质与氢键无关的是( )
A.冰的密度比液态水的密度小 B.NH3易液化
C.NH3分子比PH3分子稳定 D.在相同条件下,H2O的沸点比H2S的沸点高
18、A、B、C、D分别代表四种元素,如果 aAm+、bBn+、cCn-、dDm-四种离子的电子层结构相同(a、b、c、d为元素的质子数),下列关系正确的是( )
A.a-c=m-n B.a-b=n-m C.c-d=m+n D.b-d=n+m
17、已知在25℃,101kPa下,l gC8H18(辛烷)燃烧生成二氧化碳和液态水时放出48.40kJ热量。表示上述反应的热化学方程式正确的是( )
A.C8H18(1)+22.5O2(g)=8CO2(g)+9H2O(g)△H=-48.40kJ·mol-1
B.C8H18(1)+22.5O2(g)=8CO2(g)+9H2O(1)△H=-5518kJ·mol-1
C.C8H18(1)+22.5O2(g)=8CO2(g)+9H2O(1)△H=+5518kJ·mol-1
D.C8H18(1)+22.5O2(g)=8CO2(g)+9H2O(1)△H=-48.40kJ·mol-1
16、元素B的最高正价和负价的绝对值之差为6,B元素和A元素原子的次外层都有8个电子,AB2在水溶液中电离出电子层结构相同的离子,则AB2是( )
A.MgF2 B.CaCl2 C.K2S D.Na2O
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com