
题目列表(包括答案和解析)
31.(4分) 按指定元素的价态变化,各写一个化学方程式(每个化学方程式只能用一次)

30. (8分)下图是六种物质的相互转化关系.已知E是固态单质,六种物质中均含有构成E的元素.
(8分)下图是六种物质的相互转化关系.已知E是固态单质,六种物质中均含有构成E的元素.
(1) 写出各物质的化学式:
A: B: C:
D: E: F:
(2) 写出①④的化学方程式:
①
④
29.(2分)R2-的M电子层与L电子层的电子数目相等, 元素R应处于周期表的___周期____族.
28.(8分)A、B、C三元素原子的核外电子数都比氩原子少, A和C处于同主族, 两者间隔一周期, A元素和B元素的原子两者核电荷数之差为5, B原子核外第3电子层比第2电子层少两个电子, 则B的原子结构示意图为______;A离子的结构示意图为_____;B与C形成化合物的化学式是_____,它的电子式是 它属于 化合物(填“离子”或“共价”);A与B形成化合物的化学式是 , 它的电子式是 ,它属于 化合物。
27.(6分) 用化学符号表示符合下列条件的微粒:
(1)含有10个电子的分子有: Ne、 HF 、____、 和 CH4 。
(2)含有10个电子的阳离子有: Na+、____、____、 NH4+和 H3O+。
(3)含有10个电子的常见阴离子有:___、____、和 OH-。
26.(4分) 在O、S、Se、Te四种元素中,单质氧化性最强的化学式是___,简单阴离子还原性最强的离子符号为____. 硒元素最高价氧化物的水化物的化学式为______,它与足量的氢氧化钠溶液反应的化学方程式为_______.
25. 据报道,1994年兰州近代物理研究所研制出首批氧-18气体.氧-18(18O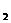 )又称重氧,下列有关叙述正确的是(NA表示阿伏加德罗常数)
)又称重氧,下列有关叙述正确的是(NA表示阿伏加德罗常数)
A. 11.2 L重氧所含分子数为0.5NA B. 36g重氧气体所含原子数为2NA
C. 2g重氧水(H218O)所含中子数为NA D. 1.8g重氧气体的物质的量为0.1mol
化学第二卷(非选择题、共50分)
24. 已知R2-离子的核内有n个中子,R的质量数为M,则mgR2-离子里含有电子的物质的量为
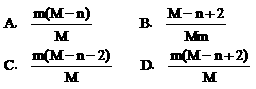
23. 关于浓硫酸的叙述错误的是
A.常温下可使金属Fe钝化,故可用铁制器皿盛装浓硫酸
B.在加热条件下可将木炭氧化,其还原产物为CO2和SO2
C.是难挥发的粘稠液体 D.不具有酸性
22. 钋是原子序数最大的氧族元素,推测钋及钋的化合物最不可能具有的性质是:
A.钋是能导电的固体 B.钋与氢气不能直接化合
C.钋的氢化物很稳定 D.钋的熔点较高
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com