
题目列表(包括答案和解析)
7.下列变化需要加入氧化剂才能发生的( )

 A.Cu2+ Cu
B.Cl― Cl2
A.Cu2+ Cu
B.Cl― Cl2

 C.H2SO4 SO2
D.CO2 CO
C.H2SO4 SO2
D.CO2 CO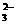
6.下列各组离子中,在水溶液中能大量共存的是( )
A.K+、H+、SO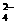 、OH-
B.Na+、Ca2+、CO
、OH-
B.Na+、Ca2+、CO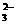 、NO
、NO
C.Na+、H+、Cl-、CO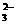 D.Na+、Cu2+、Cl-、SO
D.Na+、Cu2+、Cl-、SO
5.在5NH4NO3 == 2HNO3 + 4N2↑+ 9H2O中,被氧化的氮原子与被还原的氮原子的个数比为( )
A.3∶5 B.5∶5 C.5∶3 D.5∶8
4.已知反应“C + CO2 == 2CO”是吸热反应,下列说法正确的是( )
A.C和CO2的总能量大于CO的总能量
B.CO的总能量大于C和CO2的总能量
C.C和CO2的总能量等于CO的总能量
D.以上叙述都不对
3.下列物质中,既能与盐酸反应、又能与烧碱溶液反应的是( )
A.Na2CO3 B.NaHCO3 C.CuCl2 D.CaCO3
2.下列说法正确的是( )
A.液态HCl、固体NaCl均不导电,所以HCl、NaCl均是非电解质
B.NH3、CO2的水溶液均能导电,所以NH3、CO2均是电解质
C.铜、石墨均能导电,所以它们是电解质
D.蔗糖、酒精在水溶液或熔化时均不导电,所以它们是非电解质
1.下列说法中不正确的是( )
A.分解反应不一定是氧化还原反应
B.氧化剂具有氧化性
C.非金属单质在氧化还原反应中一定做氧化剂
D.还原剂在反应中被氧化具有还原性
22.某温度下22%NaNO3溶液150 mL,加100g水稀释后溶质的质量分数变成14% 。求:
(1)原溶液的质量
(2)原溶液的物质的量浓度
21.实验室用固体烧碱配制500mL 0.1mol·L-1的NaOH溶液。
(1)需称量______ ____ g的烧碱固体,固体应放在____________中称量。
(2)配制过程中,不需要使用的仪器是(填代号)_____________。
①烧杯 ②量筒 ③玻璃棒 ④1000mL容量瓶 ⑤漏斗
(3)根据实验的实际需要和(2)中列出的仪器判断,完成实验还缺少的仪器是____________________________________________ (填仪器名称)。
(4)①如果没有用蒸馏水洗涤烧杯、玻璃棒,配成的溶液中实验物质的量浓度比要求的_____ (填“偏高”或“偏低” );②有位同学在定容时不小心多加了水使液面高于刻度线,于是他用胶头滴管吸出过多的上层溶液。这样将会使配得的溶液的物质的量浓度 (填“偏高”、“偏低”或“无影响” )。
20.(8分)有一包白色粉末状混合物,可能含有Na2CO3、NaCl、CaCO3、CuSO4、KCl、Na2SO4、MgCl2、KNO3中的一种或几种,现进行如下实验:
(1)将混合物溶于水,得到无色透明溶液。
(2)取少量上述溶液两份,其中一份加入BaCl2溶液,立即产生白色沉淀,再加入稀硝酸,沉淀不溶解,在另一份中加入NaOH溶液,也产生白色沉淀。
根据上述实验现象回答 ①原混合物中肯定没有_________ _
②原混合物中肯定有___________ _
③不能确定是否含有_________ ____
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com