
题目列表(包括答案和解析)
10、主族元素在周期表中的位置取决于该元素原子的
A、相对原子质量和核外电子数 B、相对原子质量和最外层电子数
C、电子层数和最外层电子数 D、电子层数和次外层电子数
9、下列有关离子方程式的书写中正确的是
A、硫酸铜溶液中加入氢氧化钠:Cu2+
+ NaOH = Cu(OH)2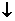 +Na+
+Na+
B、将氢氧化铝溶解于盐酸溶液中: OH- + H+ = H2O
C、金属钠与水反应: Na + 2 H2O
= Na+ + 2 OH- + H2
D、将氧化铝溶解于氢氧化钠溶液中: Al2O3 + 2 OH- = 2 AlO2- + H2O
8、下列叙述中正确的是
A、离子化合物中不一定含有金属元素
B、同周期元素的原子半径越小, 越容易失去电子
C、同周期非金属元素的原子半径越小, 气态氢化物的稳定性越弱
D、离子化合物都属于强电解质, 一定都易溶解于水
7、在下列单质中,属于半导体的是
A、O2 B、S C、Se D、Te
6、下列叙述中正确的是
A、两种粒子, 若核外电子排布完全相同, 则其化学性质完全相同
B、因为甲烷分子中碳氢键是极性键,所以甲烷为极性分子
C、两个原子, 如果核外电子排布相同, 则一定属于同种元素
D、阴离子的核外电子排布一定与上一周期稀有气体元素原子的核外电子排布相同
5、A和B为短周期元素, A- 和 B2+ 具有相同的电子层结构, 下列比较中正确的是
A、原子半径 A > B B、离子半径 A- > B2+
C、原子的中子数 A > B D、原子序数 A > B
4、某元素的一种同位素可以用符号 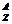 X 表示, 则该原子的中子数为
X 表示, 则该原子的中子数为
A、Z B、A C、A–Z D、A + Z
3、某主族元素R的最高正价与最低负价的代数和为4,由此可以判断
A、R一定是第四周期元素
B、R一定是IIA族元素
C、R的气态氢化物比同周期其他元素气态氢化物稳定
D、R的气态氢化物化学式为H2R
2、下列物质中,既含有离子键,又含有非极性共价键的是
A、Na2O2 B、NaOH C、CaCl2 D、H2O2
1、人类探测月球发现,在月球的土壤中含有较丰富的质量数为3的氦,它可以作为未来核聚变的重要原料之一。氦的这种同位素表示为:
A、4 3He B、3 2He C、2 4He D、3 3He
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com