
题目列表(包括答案和解析)
1. 下列说法中,不准确的是
A. 燃烧不一定要有氧气参加,但燃烧一定是放热反应
B. 化学反应中的能量变化都表现为热量变化
C. 为保证燃料充分燃烧,通入的空气要适当过量而不是越多越好
D. 为使液体燃料充分燃烧,可以将液体燃料以雾状喷出,这保证了燃料与空气有足够大的接触面积。
28、(5分)在一个定容积的密闭容器中,当温度高于100℃时测得容器内CO和H2的混合气体密闭为dg•L-1,加入适量O2恰好用完且使H2、CO完全转变为CO2和H2O,当恢复到原来状况时,其密度为4 dg•L-1。求原混合物气体中CO、 H2的体积比。
27、(9分)用200g36.5%的盐酸(过量)与17.4gMnO2反应,试回答下列问题:
(1)理论上能产生标准状况下的氯气多少体积?
(2)将反应后剩余的溶液过滤,再将虑液用水稀释至500ml,则稀释后的溶液Cl的物质的量浓度是多少?
(3)将稀释液取出100ml,加入足量的AgNO3溶液,可生成多少克白色沉淀?
26、(10分)实验室欲配制100mL0.92mol•L-1的H2SO4溶液
(1)需要用到的仪器,除了烧杯、西瓶(内盛蒸馏水)、空试剂瓶、玻璃棒、量筒、还必须有
;
(2)若提供的是18.4 mol•L-1的浓H2SO4,求所需量取的浓H2SO4的体积 mL;
(3)对配制过程中的下列说法,正确的是 。(填序号)
A.量筒量取浓硫酸后要冲洗并将冲洗液一起倒入小烧杯
B.量好体积、的浓硫酸应先倒入小烧杯中然后再加水稀释
C.稀释好的稀硫酸要立即转移入容量瓶
D.若定容后摇匀液面又下降了。则必须再补加水至刻度线。
(4)配制稀硫酸的容量瓶必须洗涤,若用刚配制过NaCl溶液的容量瓶未洗涤就配制稀硫酸,则所配稀硫酸浓度将 (偏高、偏低、不变);若用刚配制过NaOH溶液的容量瓶未洗涤就配制稀硫酸,则所配制的稀硫酸溶液的浓度将 (偏高、偏低、不变);若用刚配制过HCl溶液的容量瓶未洗涤就配制稀硫酸,则所配制稀硫酸浓度将 (偏高、偏低、不变),氢离子浓度将 (偏高、偏低、不变)。
25、(7分)根据图①、图②回答下列问题:
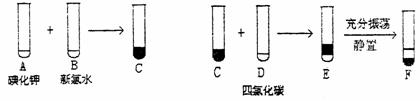
(1)A和B反应的化学方程式为 。
(2)四氧化碳是 色,比水 的液体。
(3)F中下层液体的颜色为 色,上层液体中溶质的主要成分为 。
(4)分离F中的两种液体通常应在 中进行(填仪器名称)。
24、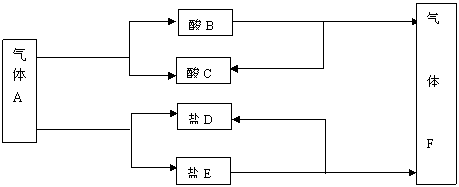 (8分)已知A、B、C、D、E、F六种物质之间有如图所示的转化关系,其中固体X是E受热分解反应的催化剂。
(8分)已知A、B、C、D、E、F六种物质之间有如图所示的转化关系,其中固体X是E受热分解反应的催化剂。
(1)试写出各物质的化学式
A B C D E F 。
(2)amolA无论按途径(I),还是按途径(II),只要完全反应,最终产生F的物质的量均为 mol,请从得失电子守恒的角度分析其原因 。
23、(8分)在标准状况下,有①4.8gCH4;②11.2LHCl;③2.408×1023个H2S气体分子;④0.2molNH3.对于这四种气体而言,请用序号比较下列各项的大小;
(1)含氢原子数由多到少的顺序为: ;(2)质量由大到小的顺序为: 。
(3)体积由大到小的顺序为: ;(4)密度由大到小的顺序为: 。
22、(8分)(1)右图是等质量的Na2CO3 、NaHCO3 粉末分别与足量的盐酸反应发生时的情景,产生CO2 气体的体积较少的试管中加入的固体试剂是 ,当反应结束时,A、B;两试管中消耗盐酸的物质的量之比为 。

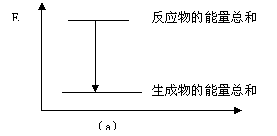 (2)实验过程中我们还能感受到Na2CO3
与盐酸反应时是放热反应,而NaHCO3
与盐酸反应时表现为吸热。在A、B两试管中,反应体系的能量变化的总趋势分别对应于A-( ),B-( )。(在括号内填写a或b)
(2)实验过程中我们还能感受到Na2CO3
与盐酸反应时是放热反应,而NaHCO3
与盐酸反应时表现为吸热。在A、B两试管中,反应体系的能量变化的总趋势分别对应于A-( ),B-( )。(在括号内填写a或b)
21、(5分)请用下列物质的序号填空:
A.Na2O2 B. Na2CO3 C. NaHCO3 D.K- Na合金
E.Na F.Ca(ClO)2 G. Ca CO3 H. NaCl
(1)可用于潜艇中供氧剂的是 ;
(2)可用于消毒饮用水的是 ;
(3)可用作原子反应堆的导热剂是 ;
(4)可用作制取发酵粉或用于治疗胃酸过多的药物的是 ;
(5)广泛用于玻璃、制皂、造纸、纺织工业上的是 。
20、用质量分数为 的浓盐酸(其密度为
的浓盐酸(其密度为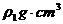 )按浓盐酸与水的体积比为1:3配制成系盐酸(其密度为
)按浓盐酸与水的体积比为1:3配制成系盐酸(其密度为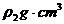 ),则随配制稀盐酸的物质的量浓度为
),则随配制稀盐酸的物质的量浓度为
A.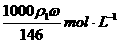 B.
B. 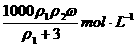
C. 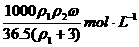 D.
D.
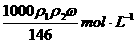
第II卷(非选择题 共60分)
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com