
题目列表(包括答案和解析)
25、核外电子分层排布的一般规律是:各电子层最多容纳的电子数为____个,最外层电子数目不超过______个,次外层电子数目不超过_____个,倒数第三层电子数目不超过_____个,核外电子总是尽先排在能量_____的电子层里,然后由里往外,依次排布在能量逐步______的电子层里。
26、带有2个单位正电荷的粒子“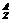 X2+”,其中A是137,中子数是81。那么该粒子的核电荷数是_______,核外电子数是_______。
X2+”,其中A是137,中子数是81。那么该粒子的核电荷数是_______,核外电子数是_______。
24.A、B、C、D四种短周期元素,原子序数D>A>B>C,且A、B同周期,C、D同主族,A的原子结构示意图为: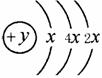 ,B、C可形成离子化合物B3C2,据此填空:
,B、C可形成离子化合物B3C2,据此填空:
(1)A的元素名称为 ,其气态氢化物的化学式为 。
(2)A、B、C、D四种元素的原子,半径由小到大的顺序为 。
(3)B和C最高价氧化物的水化物化学式分别为 和 。
23.有A、B、C、D、E五种微粒,其中A、B、C、D组成中有氢元素,且电子总数均为10个,A是双原子的阴离子,它们之间能发生下列变化:
(1)A+B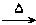 C+D↑
(2)C+Na
C+D↑
(2)C+Na  A+E
(3)D+H+
A+E
(3)D+H+ B
B
由此可知它们的化学式分别为:
A ,B ,C ,D ,E 。
22.已知X+、Y2+、Z-、W2-四种离子均具有相同的电子层结构。下列关于X、Y、Z、W四种元素的描述,不正确的是( )
A.原子半径:X>Y>Z>W B.原子序数:Y>X>Z>W
C.原子最外层电子数:Y>X>Z>W D.金属性:X>Y,还原性:W2->Z-
21.有物质的量相等的短周期金属元素单质A和B,在A中加入足量盐酸,在B中加入足量稀硫酸,反应完全后,生成氢气的体积分别为V1和V2,且V1≠V2,若要确定生成物中A和B的化合价,至少还需要的数据是( )
A.V1∶V2的值 B.V1和V2的值
C.A和B的物质的量 D.盐酸和稀硫酸的浓度
20.能说明A元素非金属性比B元素非金属性强的是( )
A.A原子得到电子的数目比B原子少
B.A元素的最高正价比B元素的最高正价要高
C.气态氢化物溶于水后的酸性:A比B强
D.A单质能与B的氢化物水溶液反应,生成B单质
19. 饱和氯水长期密封放置后,下列微粒在溶液中不会明显减少的是( )
A. Cl2 B. HClO C. ClO- D. Cl-
18. 在标准状况下,a L HCl气体溶于1000g水中,得到盐酸的密度为b g/cm3,则该盐酸的物质的量浓度为( )
A.a/22.4 mol/L B.ab/22400 mol/L
C.ab/(22400+36.5a) mol/L D.1000ab/(22400+36.5a) mol/L
17.下列变化中,必须加入氧化剂才能发生的是( )
A.SO2→S B.SO32-→SO2 C.I-→I2 D.HCO3-→CO32-
16.下列各组中的离子能在溶液中大量共存的是( )
A.K+、 H+、SO42-、OH- B.Na+、Cu2+、Cl-、 SO42-
C.Na+、H+、Cl-、 CO32- D.Na+、Ca2+、CO32-、NO3-
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com