
题目列表(包括答案和解析)
3.把Cu片插入硝酸银溶液中 4.有O2生成的分解反应
1.有H2O生成的化合反应 2.有H2O生成的分解反应
20.(12分) 写出符合下列条件的化学反应方程式,是氧化还原反应的标出电子转移的方向和数目,指出还原剂和还原产物。
19.(6分)一些酸在反应中可以表现出多种性质,如:MnO2+4HCl(浓) == MnCl2+Cl2↑+2H2O中的HCl既表现出酸性又表现出还原性,分析下列反应中酸的作用.
(1) NaOH+HCl==NaCl+H2O
____________________;
(2)C+2 H2SO4 == CO2↑+2 SO2↑+2H2O
_____________________;
(3)Cu+4HNO3 (浓)==Cu(NO3)2+2 NO2↑+2H2O
______________________。
18.(12分)配平下列氧化还原反应方程式,回答有关问题.
(1) Cl2 + KOH → KCl + KClO3 + H2O
氧化剂 ,还原剂是 ;
(2) KClO3 + HCl → Cl2 + H2O + KCl
HCl的作用是 ,被还原的元素是 .
17.(16分)在反应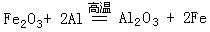 中,______元素的化合价升高,该元素的原子______电子,被________;______元素的化合价降低,该元素的原子______电子,被_________;该反应中,___________是氧化剂,___________是氧化产物。
中,______元素的化合价升高,该元素的原子______电子,被________;______元素的化合价降低,该元素的原子______电子,被_________;该反应中,___________是氧化剂,___________是氧化产物。
16. 今有下列三个氧化还原反应:
①2FeCl3+2KI==2FeCl2+2KCl+I2 ②2FeCl2+Cl2==2FeCl3
③2KMnO4+16HCl==2KCl+2MnCl2+8H2O+5Cl2↑
若某溶液中有Fe2+和I-共存,要氧化除去I-而又不影响Fe2+和Cl-,可加入的试剂是 ( C )
A. Cl2 B. KMnO4 C. FeCl3 D. HCl
15.根据下列反应判断有关物质还原性由强到弱的顺序是 ( A )
H2SO3+I2+H2O==2HI+H2SO4 2FeCl3+2HI==2FeCl2+2HCl+I2
3FeCl2+4HNO3==2FeCl3+NO↑+2H2O+Fe(NO3)3
A. H2SO3>I->Fe2+>NO B. I->Fe2+>H2SO3>NO
C. Fe2+>I->H2SO3>NO D. NO>Fe2+>H2SO3>I-
14.单质X和Y相互反应生成X2+Y2-。现有下列叙述:①X被氧化、②X是氧化剂、③X具有氧化性、④Y2-是还原产物、⑤Y2-具有还原性、⑥X2+具有氧化性、⑦Y的氧化性比X2+的氧化性强,其中正确的是 (B )
A. ①②③④ B. ①④⑤⑥⑦ C. ②③④ D. ①③④⑤
13.用下列方法:①KMnO4受热分解 ②KClO3受热分解(用MnO2作催化剂)
③2H2O2 2H2O+O2↑ ④2Na2O2+2H2O==4NaOH+O2↑,
2H2O+O2↑ ④2Na2O2+2H2O==4NaOH+O2↑,
若要制得相同质量的氧气,上述四种方法中所转移的电子数目之比是 ( D )
A. 3:2:1:4 B. 1:1:1:1 C. 1:2:1:2 D. 2:2:1:1
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com