
题目列表(包括答案和解析)
26.(7分)将1.92g铜置入一定量的浓硝酸中,并微热,随着铜的不断减少,反应生成的气
体颜色逐渐变浅,当铜反应完毕时(铜片完全消失),共收集到1.12L气体(标准状况),求:
(1)收集到的气体中含有 。
(3)反应中被还原的HNO3的物质的量是 mol。
(3)将收集上述气体的容器倒扣在盛有水的水槽中,并向其中缓慢通入O2,使其充分反应,若要使水恰好充满容器,理论上需要通入O2的体积(标准状况)是多少?
25.(4分)
(1)在12g某二价金属的硫酸盐中,含有0.4mol氧原子,此硫酸盐的摩尔质量为
g·mol-1。
(2)质量分数为49%的硫酸溶液,其密度为1.8g/cm3,则其物质的量浓度为
mol·L-1。
24.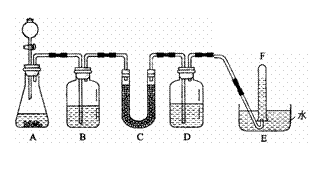 (8分)在潜水艇中可用过氧化钠作为供氧剂。请选用适当的化学试剂和实验用品,用下图中的实验装置进行实验,证明过氧化钠可用于制取氧气。
(8分)在潜水艇中可用过氧化钠作为供氧剂。请选用适当的化学试剂和实验用品,用下图中的实验装置进行实验,证明过氧化钠可用于制取氧气。
(1)A是用CaCO3制取CO2的装置。写出A中发生反应的化学方程式:
。
(2)按要求填写表中空格:
|
仪器编号 |
盛放的试剂 |
加入该试剂的目的 |
|
B |
饱和NaHCO3溶液 |
|
|
C |
|
|
|
D |
|
吸收未反应的CO2气体 |
(3)试管F中收集满气体后,下一步实验操作是
,证明收集到的气体是氧气的方法是 。
23.(6分)某校的研究性学习小组进行测定混合物各组分质量比的研究,甲、乙、丙三位同学各设计了一种实验方案如下表所示:(混合物的质量事先已称量好)
|
实验 序号 |
混合物 |
第一步:加入适量水,充分溶解 |
第二步:加入或通入的试剂 |
第三步:过滤后洗涤干燥所得固体 |
第四步:蒸发滤液得到晶体 |
第五步:称量,记录数据 |
|
甲 |
BaCl2 NaCl |
澄清溶液 |
过量CO2 |
无固体 |
晶体 |
称量所得 晶体 |
|
乙 |
CaCl2 NaCl |
澄清溶液 |
过量饱和 Na2CO3溶液 |
CaCO3 |
NaCl |
称量蒸发 所得晶体 |
|
丙 |
Na2SO4 MgSO4 |
澄清溶液 |
过量NaOH 溶液 |
|
|
|
试回答下列问题:
①你认为甲同学设计的实验步骤中,根据称量所得到的数据, (填“能”或“不能”)准确计算出混合物中各组分的质量比。
②经讨论大家认为,乙同学所设计的实验步骤的第四步填写一定有错误。其原因是什么? 。
③丙同学对实验进行了较合理的设计,将其后三步相应内容仿照前面的形式填入对应的空格内。
 21.(10分)室温下,单质A、B、C分别为固体、黄绿色气体、无色气体。在合适的条件下,它们按下图进行转化,D溶液为棕黄色,E溶液无色,F溶液为浅绿色。
21.(10分)室温下,单质A、B、C分别为固体、黄绿色气体、无色气体。在合适的条件下,它们按下图进行转化,D溶液为棕黄色,E溶液无色,F溶液为浅绿色。
请回答下列问题:
(1)B、C分别是 、 。
(2)反应①的化学方程式是 。
(3)反应④的离子方程式是 。
(4)反应⑤的离子方程式是 。
22.(10分)X、Y、Z和W分别代表四种短周期元素,其原子序数依次增大,它们满足以下条件:
①X元素的一种原子,其原子核就是一个质子
②元素周期表中,Z与Y相邻,Z与W相邻
③Y、Z与W三种元素的原子最外层电子数之和为17
④由X、Y元素组成的一种气体物质A,A能使湿润的红色石蕊试纸变蓝色
请填以下空白:
(1)Y、Z和W三种元素是否位于同一周期(填“是”或“否”): ,理由是 。
(2)写出四种元素的元素符号:X ,Y ,Z ,W ,
(3)实验室制取气体A的化学反应方程式为 ;
干燥A气体应选用的试剂是 ;收集A可用 法。
20.(2分)金属镁被誉为“国防金属”,若镁起火,不能用CO2来灭火,其原因可用化学方程式表示为 。
19.(6分)Na2CO3固体中混有少量NaHCO3杂质,除去杂质的方法是 ,反应的化学方程式为 ;若NaHCO3溶液中混有少量Na2CO3杂质,除去杂质的方法是 。
18.(共6分)在同温同压下,在相同体积的CO和CO2中,分子个数之比为 ,氧原子个数之比为 ,密度之比为 。
17.把4.48L CO2通过一定量的固体过氧化钠后收集到3.36L气体(气体的测量均在标准状况下),则这3.36L气体的质量是 ( )
A.6.0g B.5.6g C.4.8g D.3.8g
|
15.在一定温度下,向饱和苛性钠溶液中放一定量的过氧化钠,充分反应后恢复到原温度,下列有关说法中,正确的是 ( )
A.溶液中Na+浓度增大,有O2放出 B.溶液pH不变,有H2放出
C.溶液中Na+数目减少,有O2放出 D.溶液中pH增大,有O2放出
 16.某溶液中可能含有大量的Mg2+、Al3+、H+、Cl-和少量OH-,向该溶液中逐滴加入0.5mol·L-1的NaOH溶液,生成沉淀的质量和加入NaOH溶液的体积之间的关系如下图所示,则可判断原溶液中 ( )
16.某溶液中可能含有大量的Mg2+、Al3+、H+、Cl-和少量OH-,向该溶液中逐滴加入0.5mol·L-1的NaOH溶液,生成沉淀的质量和加入NaOH溶液的体积之间的关系如下图所示,则可判断原溶液中 ( )
A.有Mg2+,没有Al3+
B.有Al3+,没有Mg2+
C.有大量的H+、Mg2+和Al3+
D.有Mg2+和Al3+
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com