
题目列表(包括答案和解析)
2.强电解质和弱电解质的本质区别在于 ( )
A.强电解质易溶于水,弱电解质难溶于水 B.相同浓度时,溶液导电能力的强弱
C.在水溶液里电解质是否全部电离为离子 D.是离子化合物还是共价化合物
1.下列叙述正确的是 ( )
A.氧化还原反应的本质是化合价发生变化
B.氧化剂在同一反应中既可以是反应物,也可以是生成物
C.有单质产生的分解反应一定是氧化还原反应
D.还原剂在反应中发生还原反应
38. 某校学生课外活动小组的同学设计如下图所示实验装置,用来验证一氧化碳具有还原性。回答下列问题:
某校学生课外活动小组的同学设计如下图所示实验装置,用来验证一氧化碳具有还原性。回答下列问题:

(1)装置B中最适宜的试剂是NaHCO3,其作用是
(2)若实验中没有装置C,则不可以证明CO具有还原性,原因是:
(3)用化学方程式表示装置D的作用为
(4)根据实验中的 现象,可证明CO具有还原性。
37.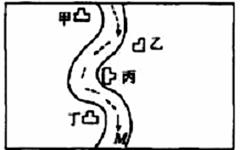 在一条鱼、虾绝迹的小河边有四座工厂:甲、乙、丙、丁(如右图所示),它们排出的废液里,每个工厂只含有 Na2CO3、FeCl3。、Ca(OH)2、HCl中的一种。某中学环保小组对河水监测时发现:①甲处河水呈乳白色,②乙处河
在一条鱼、虾绝迹的小河边有四座工厂:甲、乙、丙、丁(如右图所示),它们排出的废液里,每个工厂只含有 Na2CO3、FeCl3。、Ca(OH)2、HCl中的一种。某中学环保小组对河水监测时发现:①甲处河水呈乳白色,②乙处河
水呈红褐色,③丙处河水由浑变清,④丁处产生气泡,
河水仍清。请推断:
(1)四座工厂排出的废液里含有的污染物:
甲 ,丙 。
(2)小河中鱼虾几乎绝迹的原因是
。
36.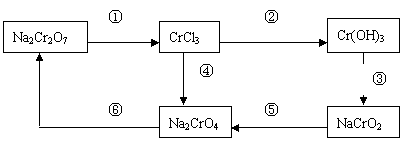 化学实验中,如使某步骤中的有害产物作为另一步的反应物,形成一个循环,就可不再向环境排放该种有害物质,如图所示物质转化关系:
化学实验中,如使某步骤中的有害产物作为另一步的反应物,形成一个循环,就可不再向环境排放该种有害物质,如图所示物质转化关系:
(1)上述各步骤中,需用还原剂的是 需用氧化剂的是 (以上两空均填编号)
(2)在Na2Cr2O7+6FeSO4 +7H2SO4(浓)= 3Fe2(SO4)3+ Cr2(SO4)3 +Na2SO4 + 7H2O中,电子转移总数为
35.按要求配平下列化学或离子反应方程式:
(1) FeSO4+ HNO3+ H2SO4=== Fe2(SO4)3+ NO↑+ H2O
(2) MnO4-+ H2S+ H+ === Mn2++ S↓+ H2O
(3) Cu2++SO42-+ + ===Cu(OH)2↓+
34.已知:2A3+ +2B-=2A2+ + B2,C2 +2A2+ =2A3+ +2C-,2C-+D2 = C2 + 2D-。现向含有A2+、
B-、C-、D-的溶液中加入足量的C2,则反应后溶液中离子数量明显减少的是 ,
离子数量基本不变的是 ,离子数量明显增多的是 ,
33.现有下列物质:①NaCl晶体 ②液态SO2 ③液态的醋酸 ④汞 ⑤BaSO4固体
⑥纯蔗糖(C12H22O11) ⑦酒精(C2H5OH) ⑧KOH溶液 (以下各空均填序号)
(1)以上能导电的是 (2)以上属强电解质的是
(3)以上属非电解质的是 。
32.在S2-、 Fe2+、Fe3+、Mg2+、S、I-、H+中,只有氧化性的是 ,只有还原性的是 ,既有氧化性又有氧化性的是
31.仔细观察右图后回答:
该图反映的环境问题是 ;
请你提一条合理化建议 。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com