
题目列表(包括答案和解析)
5.下列反应中H2SO4既表现氧化性又表现酸性的是 ( )
A.2KOH+H2SO4=K2SO4+2H2O B.C+2H2SO4(浓) CO2↑+2SO2↑+2H2O
CO2↑+2SO2↑+2H2O
C.H2S+H2SO4(浓)= S↓+SO2↑+2H2O D.Cu+2H2SO4(浓)  CuSO4+SO2↑+2H2O
CuSO4+SO2↑+2H2O
4.关于反应C+CO2 == 2CO,下列说法正确的是 ( )
A、是化合反应,不是氧化还原反应
B、CO既是氧化产物又是还原产物
C、单质C中C的化合价升高,被还原,是氧化剂
D、CO2中C的化化合价降低,被氧化,CO2是还原剂
3.为了更好地解决能源问题,人们一方面研究如何提高燃料的燃烧效率,另一方面寻找新能源,下面与提高燃料的燃烧效率无关的是
A.煤的气化与液化 B.液体燃料雾状喷出
C.集中烘热 D.使用太阳能
2.下列反应中,不属于氧化还原反应的是 ( )
A、2CO+O2  2CO2
B、CH4+2O2
2CO2
B、CH4+2O2 CO2+2H2O
CO2+2H2O
C、2KClO3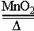 2KCl+3O2↑ D、2Fe(OH)3
2KCl+3O2↑ D、2Fe(OH)3 Fe2O3 +3H2O
Fe2O3 +3H2O
1.氧化还原反应的实质是 ( )
A.氧元素的得与失 B.化合价的升降C.电子的得失或偏移 D.分子中原子重新组合
20.(8分)已知一定条件下硫化氢与二氧化硫反应生成硫和水,反应方程式为2H2S+SO2=3S↓+2H2O,反应中若被氧化与被还原的硫质量差为3.2g,则参加反应的氧化剂质量为多少克?
19.(12分)一学生设计右图所示装置进行NaHCO3的分解,并证实产物中有CO2产生。
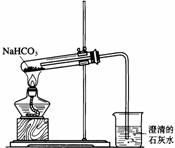 (1)试管中发生的化学反应方程式是
(1)试管中发生的化学反应方程式是
(2)指出该学生设计的装置图的错误之处,并改正(文 字说明即可)。(至少2处)
(3)烧杯中发生反应的离子方程式是_______________________________
(4)如果将16.8gNaHCO3加热一段时间,然后将剩余固体溶于水,并加入足量的CaCl2溶液,最终得到白色沉淀5.0g,则NaHCO3分解百分率为______________,加CaCl2后反应的离子方程式为______________________________________________________。
18.(6分)某无色溶液中可能含有Ca2+、Cl-、CO32-、SO42-、Na+、MnO4-中的一种或几种,现做以下实验确定其组成:
(1)取少量溶液加入足量BaCl2溶液,产生大量白色沉淀,过滤。
(2)取上述白色沉淀加入足量稀HCl,沉淀部分溶解。
(3)取少量(1)中溶液加入AgNO3溶液和稀HNO3,产生白色沉淀不溶解。
根据上面实验知原溶液中肯定有____________离子,肯定没有____________离子,可能有____________离子。
17.(10分)2008年9月25日21时10分,我国在酒泉卫星发射基地成功发射神舟七号宇宙飞船,实现了中国航天航空史上的伟大突破。承载神舟七号升空任务的是由长征二号F型火箭,其第一节、第二节、第三节均以液态四氧化二氮和联氨(N2H4)为原料,使后者在前者中燃烧,产生巨大的推动力助火箭升空,最终产物是N2和H2O。
(1)请写出该反应的化学方程式__________________________________________
(2)反应中氧化剂是____________,氧化产物与还原产物质量比为_____________。
(3)该反应的类型判断正确的是_______
a.氧化还原反应 b.离子反应 c.置换反应 d.放热反应 e.分解反应
(4)标出该反应中电子转移的方向和数目:_______________________。
16.(10分)在加热氯酸钾的分解反应中,二氧化锰作催化剂的问题,到目前还没有肯定的解释。鉴于制得的氧气里有氯气的气味,生成的氯化钾带紫红色,认为反应过程如下:
①2KClO3+2MnO2=2A+B↑+C↑ ②2A=D+MnO2+C↑ ③B+D=2KCl+MnO2+C
(1)写出A、B、C、D的化学式:A________,B________,C________,D________。
(2)第①步反应中,氧化产物是(填化学式)_______,被还原的元素是(填元素符号)__________。
(3)在上述①②③三步反应中若产生3个C分子,电子转移总数为 ________e-。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com