
ƒø¡–±Ì(∞¸¿®¥∞∏∫ÕΩ‚Œˆ)
15°¢(6∑÷)”√œ¬√Ê¡Ω÷÷∑Ω∑®ø…“‘÷∆µ√∞◊…´µƒFe(OH)2≥¡µÌ°£
∑Ω∑®“ª£∫”√≤ª∫¨Fe3+µƒFeSO4»Ð“∫”Δ√≤ª∫¨O2µƒ’Ù¡ÛÀÆ≈‰÷∆µƒNaOH»Ð“∫∑¥”¶÷∆±∏°£
¢≈≥˝»•’Ù¡ÛÀÆ÷–»ÐΩ‚µƒO2≥£≤…”√°°°° °°°°°°°°µƒ∑Ω∑®°£
 ¢∆…˙≥…∞◊…´Fe(OH)2≥¡µÌµƒ≤Ÿ◊˜ «”√≥§µŒπÐŒ¸»°≤ª∫¨O2µƒNaOH»Ð“∫£¨≤»ÎFeSO4°° »Ð
¢∆…˙≥…∞◊…´Fe(OH)2≥¡µÌµƒ≤Ÿ◊˜ «”√≥§µŒπÐŒ¸»°≤ª∫¨O2µƒNaOH»Ð“∫£¨≤»ÎFeSO4°° »Ð
“∫“∫√Êœ¬£¨‘Ÿº∑≥ˆNaOH»Ð“∫°£’‚—˘≤Ÿ◊˜µƒ¿Ì”… «°°°°°°°° °°°°°°°°°°°°°°°°°°°°°°°£
∑Ω∑®∂˛£∫‘⁄»ÁÕº◊∞÷√÷–£¨”√NaOH»Ð“∫°¢Ã˙–º°¢œ°H2SO4µ» ‘º¡÷∆±∏°£
¢≈‘⁄ ‘πТҿԺ”»Îµƒ ‘º¡ «°°°°°°°°°°°° °£
¢∆‘⁄ ‘πТڿԺ”»Îµƒ ‘º¡ «°°°°°°°°°°°° °£
¢«Œ™¡À÷∆µ√∞◊…´Fe(OH)2≥¡µÌ£¨‘⁄ ‘πТÒ∫Õ¢Ú÷–º”»Î ‘º¡£¨¥Úø™÷πÀƺ–£¨»˚ΩÙ»˚◊” ∫Û
µƒ µ—È≤Ω÷Ë «°°°°°°°°°°°°°°°° °°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°
°°
°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°° °£
¢»’‚—˘…˙≥…µƒFe(OH)2≥¡µÌƒÐΩœ≥§ ±º‰±£≥÷∞◊…´£¨∆‰¿Ì”… «°°°° °°°°°°°°°°°°°°°°
°°
°°°°°°°°°°°°°°°°°°°°°°°°°° °°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°£
14°¢Œ™œ˚≥˝NOx∂‘¥Û∆¯µƒŒ€»æ£¨π§“µ…œÕ®≥£¿˚”√»Áœ¬∑¥”¶£∫NOx +NH3°˙N2 +H2O¿¥±£ª§ª∑æ≥°£œ÷”–NO2∫ÕNOµƒªÏ∫œ∆¯ÃÂ3L£¨ø…”√œýÕ¨◊¥øˆœ¬3.5LNH3«°∫√ π∆‰ÕÍ»´◊™ªØ≥…N2£¨‘ÚªÏ∫œ∆¯ÃÂ÷–NO2∫ÕNOµƒÃª˝÷Ʊ»Œ™
A°¢1 : 4°°°°°° °°°°B°¢3 : 1°°°°°° °°°°°°C°¢2 : 1°°°°°°°°°°°° D°¢1 : 1
 °°
°°
ªØ°° —ß°° ‘°° æÌ°° ¥°° °° ÷Ω°°°° (2008.11)
µ⁄°° I°° æÌ
|
1 |
2 |
3 |
4 |
5 |
6 |
7 |
8 |
|
°° |
°° |
°° |
°° |
°° |
°° |
°° |
°° |
|
9 |
10 |
11 |
12 |
13 |
14 |
°° |
°° |
|
°° |
°° |
°° |
°° |
°° |
°° |
°° |
°° |
µ⁄°° II°° æÌ
13°¢¡™∫œ÷∆ºÓ∑®÷–πÿº¸µƒ“ª≤Ω «∞—NH4Cl¥”º∏∫ı±•∫ÕµƒNaHCO3»Ð“∫÷–∑÷¿Î≥ˆ¿¥£¨Œ™¥À∏˘æðNaCl∫ÕNH4Cl»ÐΩ‚∂»µƒ≤Ó“Ï£¨œÚªÏ∫œ»Ð“∫÷–Õ®»Îƒ≥÷÷∆¯Ã£¨Õ¨ ±º”»Îƒ•œ∏µƒ ≥—Œ£¨ø…Œˆ≥ˆ≤ªº–¥¯NaHCO3µƒNH4Cl.NaCl∫ÕNH4Clπ≤Õ¨¥Ê‘⁄ ±µƒ»ÐΩ‚∂»«˙œþ»ÁÕºÀ˘ 棨“‘œ¬≤Ÿ◊˜’˝»∑µƒ «°°
|
°° |
Õ®»Î∆¯Ã |
Œ¬∂»øÿ÷∆ |
|
(A) (B) (C) (D) |
CO2 CO2 NH3 NH3 |
30~40°Ê 0~10 °Ê 30~40 °Ê 0~10°Ê |
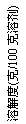
12°¢œ¬¡–Àµ∑®÷–’˝»∑µƒ «
°°A°¢∫ÀÕ‚µÁ◊”≈≈≤ºÕÍ»´œýÕ¨µƒ¡Ω÷÷Œ¢¡££¨∆‰ªØ—ß–‘÷ “ª∂®œýÕ¨
°°B°¢æþ”–πÃ∂®»€µ„ªÚ∑–µ„µƒŒÔ÷ “ª∂® «¥ø檌Ô
°°C°¢“ª÷÷¿Î◊”∫Õ“ª÷÷∑÷◊”µƒ÷ ◊” ˝∫ÕµÁ◊” ˝≤ªø…ƒÐÕ¨ ±œýµ»£ª
°°D°¢π≤º€ªØ∫œŒÔ»Ð”⁄ÀƵÁ¿Îπ˝≥Ã÷–£¨π≤º€º¸±ª∆∆ªµ°£
11°¢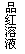

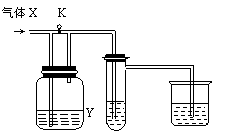 ”“Õº «“ªÃ◊ºÏ—È∆¯Ã–‘÷ µƒ µ—È◊∞÷√°£œÚ◊∞÷√÷–ª∫ª∫Õ®»Î∆¯ÃÂX£¨»Ùπÿ±’ªÓ»˚K£¨‘Ú∆∑∫ϻГ∫Õ …´°£æð¥À≈–∂œ∆¯ÃÂX∫Õœ¥∆¯∆øƒ⁄µƒ»Ð“∫Yø…ƒÐµƒ◊È∫œ «
”“Õº «“ªÃ◊ºÏ—È∆¯Ã–‘÷ µƒ µ—È◊∞÷√°£œÚ◊∞÷√÷–ª∫ª∫Õ®»Î∆¯ÃÂX£¨»Ùπÿ±’ªÓ»˚K£¨‘Ú∆∑∫ϻГ∫Õ …´°£æð¥À≈–∂œ∆¯ÃÂX∫Õœ¥∆¯∆øƒ⁄µƒ»Ð“∫Yø…ƒÐµƒ◊È∫œ «
|
°° |
A |
B |
C |
D |
|
X |
¡ÚªØ«‚ |
∂˛—ıªØ¡Ú |
∂˛—ıªØú |
¬»ªØ«‚ |
|
Y |
≈®¡ÚÀ· |
±•∫ÕNaHCO3 |
Na2SO3»Ð“∫ |
±•∫ÕNaHSO3 |
10°¢œ¬¡–¿Î◊”∑Ω≥à Ω÷–¥ÌŒÛµƒ «
A°¢œ°∞±ÀÆŒ¸ ’◊„¡øSO2£∫ NH3°§H2O + SO2 = NH4+ + HSO3-
B°¢œÚCa(ClO)2»Ð“∫÷–Õ®»Îπ˝¡ø∂˛—ıªØú£∫ClO- + H2O + CO2 = HClO + HCO3-
C°¢œ°œıÀ·÷–º”»ÎÃ˙∑€£∫2Fe + 6H+ = 2Fe3+ + 3H2°¸
D°¢π˝—ıªØƒ∆∫Õ¿‰ÀÆ∑¥”¶£∫2Na2O2 + 2H2O = 4Na+ + 4OH- + O2°¸
9°¢ƒ≥»Ð“∫÷–”–NH4+°¢Mg2+°¢Fe2+∫ÕAl3+Àƒ÷÷¿Î◊”£¨»ÙœÚ∆‰÷–º”»Îπ˝¡øµƒ«‚—ıªØƒ∆»Ð“∫£¨Œ¢»»≤¢Ω¡∞Ë£¨‘Ÿº”π˝¡ø—ŒÀ·£¨»Ð“∫÷–¥Û¡øºı…Ÿµƒ—Ù¿Î◊” «
°°A°¢NH4+°°°°°°°° B°¢Mg2+°°°°°°°°°°°°°°°° C°¢Fe2+°°°°°°°°°°°°°°°°°° D°¢Al3+
8°¢A-D «∫¨Õ¨“ª‘™ÀÿµƒÀƒ÷÷ŒÔ÷ £¨œýª•÷ƺ‰”–»Áœ¬Õºµƒ◊™ªØπÿœµ£¨∆‰÷–A «µ•÷ £¨D «◊Ó∏þº€—ıªØŒÔµƒÀƪ،԰£ƒ«√¥Aø…ƒÐ «
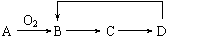 A£ÆS°°°°°°°°°°
B£ÆCl2°°
A£ÆS°°°°°°°°°°
B£ÆCl2°°
C£ÆFe°°°°°°°°°° D£ÆSi
7°¢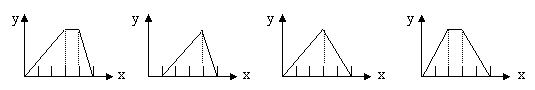 Ω´ŒÔ÷ µƒ¡øœýµ»µƒ¡ÚÀ·¬¡∫Õ¡ÚÀ·Ô߻Д⁄ÀÆ–Œ≥…VmLªÏ∫œ»Ð“∫£¨œÚªÏ∫œ»Ð“∫÷–÷µŒº”»Îƒ≥«‚—ıªØƒ∆µƒ»Ð“∫(∆‰ŒÔ÷ µƒ¡ø≈®∂»Œ™ªÏ∫œ»Ð“∫÷–¡Ω»Ð÷ µƒŒÔ÷ µƒ¡ø≈®∂»÷Æ∫Õ)£¨÷±÷¡π˝¡ø°£œ¬¡–±Ì æ«‚—ıªØƒ∆»Ð“∫º”»ÎµƒÃª˝(x)”λГ∫÷–≥¡µÌŒÔµƒ¡ø(y)µƒπÿœµ æ“‚Õº÷–’˝»∑µƒ «
Ω´ŒÔ÷ µƒ¡øœýµ»µƒ¡ÚÀ·¬¡∫Õ¡ÚÀ·Ô߻Д⁄ÀÆ–Œ≥…VmLªÏ∫œ»Ð“∫£¨œÚªÏ∫œ»Ð“∫÷–÷µŒº”»Îƒ≥«‚—ıªØƒ∆µƒ»Ð“∫(∆‰ŒÔ÷ µƒ¡ø≈®∂»Œ™ªÏ∫œ»Ð“∫÷–¡Ω»Ð÷ µƒŒÔ÷ µƒ¡ø≈®∂»÷Æ∫Õ)£¨÷±÷¡π˝¡ø°£œ¬¡–±Ì æ«‚—ıªØƒ∆»Ð“∫º”»ÎµƒÃª˝(x)”λГ∫÷–≥¡µÌŒÔµƒ¡ø(y)µƒπÿœµ æ“‚Õº÷–’˝»∑µƒ «
A°¢°°°°°°°°°°°°°°°° B°°°°°°°°°°°°°°°° C°°°°°°°°°°°°°°°°°°°° D
6°¢NO“ÚŒ€»æø’∆¯∂¯°∞≥Ù√˚’—÷¯°±£¨∂¯∆‰∆Ê√Ó◊˜”√“≤ π∆‰≥…Œ™°∞√˜–«∑÷◊”°±°£»Á÷∆œıÀ·°¢∑ ¡œ°¢’®“©°¢¥ŸΩ¯—™πп©’≈°¢¥ŸΩ¯√‚“þπ¶ƒÐ°¢‘ˆ«øº«“‰µ»°£∆‰π§“µ÷˜“™¿¥‘¥ «
A°¢ Cu+HNO3°˙°°°°°° B°¢N2+O2°˙°°°°°°°° C°¢NO2+H2O°°°°°° D°¢NH3+O2°˙
∞Ÿ∂»÷¬–≈ - ¡∑œ∞≤·¡–±Ì - ‘¡–±Ì
∫˛±± °ª•¡™Õ¯Œ•∑®∫Õ≤ª¡º–≈œ¢æŸ±®∆Ωî | Õ¯…œ”–∫¶–≈œ¢æŸ±®◊®«¯ | µÁ–≈’©∆≠柱®◊®«¯ | …Ê¿˙ ∑–ÈŒÞ÷˜“”–∫¶–≈œ¢æŸ±®◊®«¯ | …Ê∆Û«÷»®æŸ±®◊®«¯
Œ•∑®∫Õ≤ª¡º–≈œ¢æŸ±®µÁª∞£∫027-86699610 柱®” œ‰£∫58377363@163.com