
题目列表(包括答案和解析)
12.将一定质量的Zn、Fe、Mg、Al混合物与足量稀H2SO4反应,生成H22.8L(标况),原混合物的质量可能为( )
A、2g B、4g C、8g D、10g
11.将a g CuO和Fe2O3的混合物分成两等份,向其中一份中加入b mL c mol/L的稀盐酸正好完全反应;另一份在加热的条件下用H2还原,反应完全时用去H2 d L(折算成标准状况)。则d等于( )
A、11.2bc×10-3 B、22.4bc×10-3
C、22.4(3a-4bc×10-3) D、22.4(3a-4bc)×10-3
10.NaHCO3和Na2CO3·10H2O晶体的混合物10g,溶于水制成200mL溶液,其中c(Na+)=0.50mol/L。若将10g的这种混合物,加热到质量不变为止,减少的质量为( ) A、5.3g B、4.7g C、5.0g D、4.0g
9.已知氧化还原反应:2Cu(IO3)2+24KI+12H2SO4 = 2CuI↓+13I2+12K2SO4+12H2O
其中1 mol氧化剂在反应中得到的电子为( )
A.10 mol B.13 mol C.12 mol D.11 mol
8.今有一混合物的水溶液,只可能含有以下离子中的若干种:K+、NH4+、Cl-、Mg2+、Ba2+、CO32-、SO42-,现取三份100mL溶液进行如下实验:
(1)第一份加入AgNO3溶液有沉淀产生
(2)第二份加足量NaOH溶液加热后,收集到气体0.04mol
(3)第三份加足量BaCl2溶液后,得干燥沉淀6.27g,经足量盐酸洗涤、干燥后,沉淀质量为2.33g。根据上述实验,以下推测正确的是( )
A、 K+一定存在 B、 100mL溶液中含0.01mol CO32-
C、 Cl-可能存在 D、 Ba2+一定不存在,Mg2+可能存在
7.(NH4)2SO4在高温下分解,产物是SO2、H2O、N2和NH3,在该反应的化学方程式中,化学计量数由小到大的产物分子依次是( )
A. SO2、H2O、N2、NH3 B. N2、SO2、H2O 、NH3
C. N2、SO2、NH3、H2O D. H2O、NH3、SO2、N2
6.下列各组物质,可用一种试剂进行鉴别的是( )
①四种黑色固体:FeO、Fe、CuO、C
②四种白色粉末:(NH4)2SO4、NH4Cl、Na2SO4、NaCl
③四种无色溶液:乙醛、乙酸、甲酸、乙醇
④四种有机物: 苯、四氯化碳、无水乙醇、己烯
A.全部 B.只有①② C.只有③④ D.只有①②④
5.下列描述正确的是( )
A.1molNa2O2参加化学反应总是转移1mol电子
B.1molCl2参加化学反应总是转移2mol电子
C.1mol固体Na218O2与足量CO2反应后,固体质量增重26g
D.金属钾应保存在CCl4中
4.已知下列元素的半径为:
|
原子 |
N |
S |
O |
Si |
半径r/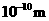 |
0.75 |
1.02 |
0.74 |
1.17 |
根据以上数据,磷原子的半径可能是( )
A.0.80×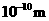 B.1.10×
B.1.10×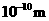 C.1.20×
C.1.20×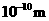 D.0.70×
D.0.70×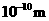
3.下列属于非电解质的是( )
A.Cl2 B.NH3 C.CH3COOH D.C6H5ONa
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com