
题目列表(包括答案和解析)
29.现有三种常见治疗胃病药品的标签:药品中所含的物质均能中和胃里过量的盐酸,下列关于三种药片中和胃酸的能力比较(单位质量),正确的是( )
A.①=②=③ B.①>②>③ C.③>②>① D.②>③>①

28.在100 mL含等物质的量的HBr和 的溶液里通入0.01mol
的溶液里通入0.01mol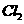 ,有一半Br-变为
,有一半Br-变为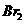 (已知
(已知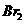 能氧化
能氧化 )。原溶液中HBr和
)。原溶液中HBr和 的浓度都是( )
的浓度都是( )
A.0.0075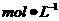 B.0.08
B.0.08 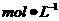 C.0.075
C.0.075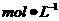 D.0.008
D.0.008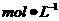
27.已知有如下反应:①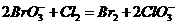 ,
,
②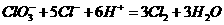 ,③
,③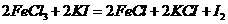 ,④
,④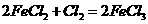 。下列各微粒氧化能力由强到弱的顺序正确的是( )
。下列各微粒氧化能力由强到弱的顺序正确的是( )
A .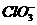 >
> >
>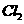 >
>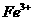 >
>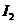 B.
B. >
>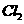 >
>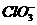 >
>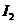 >
>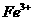
C. >
>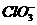 >
>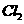 >
>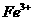 >
>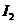 D.
D. >
>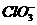 >
>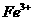 >
>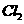 >
>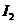
26.若 表示阿佛加德罗常数,下列说法正确的是( )
表示阿佛加德罗常数,下列说法正确的是( )
A. A个二氧化碳分子和0.5
mol甲烷的质量比为l l:4
A个二氧化碳分子和0.5
mol甲烷的质量比为l l:4
B.1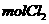 作为氧化剂得到的电子数为
作为氧化剂得到的电子数为
C.在0℃,101kPa时,11.2 L氢气中含有0.5 个氢原子
个氢原子
D.14 g氮气中含有7 个电子
个电子
25.下列各组离子能在溶液中大量共存的是( )
A .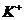 、
、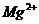 、
、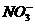 、
、 B.
B.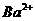 、
、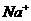 、
、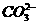 、
、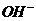
C.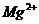 、
、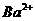 、
、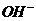 、
、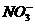 D.
D.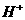 、
、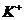 、
、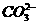 、
、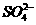
24.下列各选项的每组两种物质在溶液中反应,可用同一离子方程式表示的是( )
A.氢氧化钠与盐酸;氢氧化铜与盐酸
B.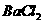 溶液与
溶液与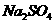 溶液;
溶液;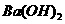 溶液与
溶液与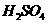 溶液
溶液
C.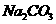 溶液与硝酸溶液;
溶液与硝酸溶液;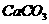 溶液与硝酸溶液
溶液与硝酸溶液
D.石灰石与硝酸反应;石灰石与盐酸
23.(1)(4分)在标准状况下,11.2 L氨气的质量为______g,含有______个氨分子。
(2)(2分)12gC与足量的浓硝酸充分反应,在标准状况F生成气体的体积为______L。
B卷(满分50分)
2l(8分)某同学用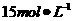 浓硫酸,按下列步骤配制
浓硫酸,按下列步骤配制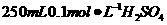 溶液,请
溶液,请
回答有关问题。
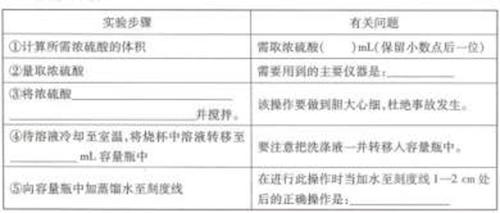
(1)本实验不需要用到的仪器是( )
a.玻璃棒 b.烧杯 c.天平 d胶头滴管
(2)在进行④步操作时,不慎将溶液溅到容量瓶外,则配制溶液的浓度将__________(填写偏高、偏低、不影响。下同)。若配制时容量瓶没有干燥,则配制溶液浓度将__________。
(2)(8分)某研究人员应用下图研究物质的性质,其中气体A的主要成分是氯气,杂质是空气和水蒸汽。请回答下列问题:
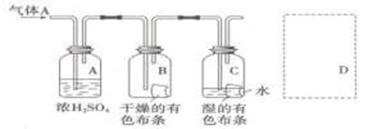
(1)浓硫酸的作用是________________________。
(2)通入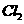 后,从集气瓶B中干燥的有色布条的现象可得出的结论是____________________________________;从集气瓶C中湿润的有色布条的现象可得出的结论是________________________________________________________________________。
后,从集气瓶B中干燥的有色布条的现象可得出的结论是____________________________________;从集气瓶C中湿润的有色布条的现象可得出的结论是________________________________________________________________________。
(3)从物质性质的方面来看,这样的实验设计还存在事故隐患,请在图D处以图的形式表明克服事故隐患的措施。
24. 若A在常温下为固态单质,则C→D变化的化学方程式为_________________________,E→C变化的化学方程式为______________________________。
23. 若A在常温下为气态单质,则A为_____;D为_____;B+E反应的离子方程式为______________________________
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com