
题目列表(包括答案和解析)
4.下列各组物质中,使有色物质褪色的反应机理相同的是
A.二氧化硫和过氧化钠 B.过氧化氢和次氯酸
C.二氧化硫和漂白粉 D.活性炭和二氧化硫
3.下列有关项目的比较中,错误的是
A.酸性:H2SiO3>H2CO3 B.氧化性:Fe3+>Fe2+
C.热稳定性:Na2CO3>NaHCO3 D.硬度:金刚石 > 刚玉
2.下列说法正确的是
A.Cl-和Cl2都是氯元素 B.Cl2有毒,Cl-也有毒
C.次氯酸中氯元素的化合价为+1 D.Cl2和Cl原子都呈黄色
1.下列表述正确的是
①开发使用新型清洁能源,减少化石燃料的燃烧,可从根本上防止酸雨的产生 ②我国从2000年起逐渐用二氧化氯取代氯气对饮用水进行消毒,因为二氧化氯杀菌、消毒能力强,持效长 ③氧化镁可用来制造耐火砖和坩埚等④明矾能使水中的悬浮物凝聚,可做为净水剂 ⑤建设三峡大坝使用了大量水泥,水泥是硅酸盐材料 ⑥给机动车安装尾气净化器,可减少光化学烟雾的发生
A.①④⑤ B.①②④⑤ C.②③④⑥ D.全部
23. (6分)将28.8克铜与100mL一定浓度的硝酸反应,恰好完全反应,产生的NO和NO2混合气体在标准状况下的体积为11.2L,请回答:
⑴ 产生的NO和NO2的物质的量分别为多少?
⑵ 求原硝酸溶液的物质的量浓度为多少?
东莞中学2008-2009学年度第一学期教学质量检查
22.(12分)工业上用铝土矿(主要成分是Al2O3,还有少量的Fe2O3、SiO2)提取冶炼铝的原料氧化铝。工艺流程如下图:
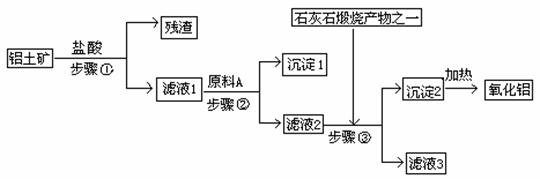
(1) 步骤①反应的离子方程式是
_____________________________ ________________
___________________________________________________________________。
(2) 滤液1中要加入稍过量原料A,原料A的化学式是________________,步骤②反应的离子方程式
_________________________________________________________________
_________________________________________________________________。
(3)步骤③所得沉淀2的化学式为:________________。
(4)如果省去步骤①,即溶解铝土矿是从加入原料A开始,则会对氧化铝的提取有什么影响?____________________________________________________________________。
21.(9分)下列反应对自然界中碳酸钙的搬运、喀斯特地貌的形成具有重要意义:CaCO3+H2O+CO2=Ca2++2HCO3-。富含二氧化碳的地下水流经大理石岩层时,通过该反应腐蚀岩层,久而久之,就形成了溶洞,溶洞还可能塌垮而形成天坑。地下河把Ca2+和HCO3-带到其他地方,渗出、滴下的水蒸发后,碳酸氢钙[Ca(HCO3)2]分解Ca(HCO3)2=CaCO3↓+H2O+CO2↑,产生的碳酸钙不断累积,就形成了钟乳石、石笋、石柱等自然景观。
(1)写出Na2CO3溶液中通入二氧化碳时反应的离子方程式:
据此,为什么除去二氧化碳气体中混有的少量氯化氢等酸性气体时,用饱和NaHCO3溶液而不用Na2CO3溶液
。
 (2)用NaOH溶液吸收二氧化碳气体,每摩尔氢氧化钠最多可吸收标准状况下
(2)用NaOH溶液吸收二氧化碳气体,每摩尔氢氧化钠最多可吸收标准状况下
升CO2。
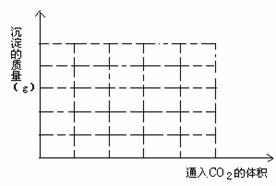
(3)向一定量的氢氧化钙溶液中慢慢通入二氧化碳气体,请在图中画出反应体系中沉淀的质量与通入二氧化碳体积之间的关系图
20.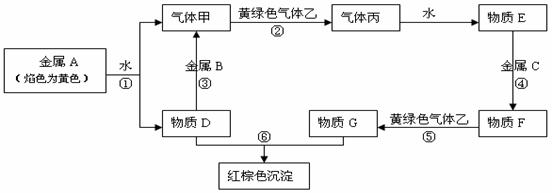 (7分)现有金属单质A、B、C和气体甲、乙、丙及物质D、E、F、G、H,它们之间能发生如下反应(图中有些反应的产物和反应的条件没有全部标出)。
(7分)现有金属单质A、B、C和气体甲、乙、丙及物质D、E、F、G、H,它们之间能发生如下反应(图中有些反应的产物和反应的条件没有全部标出)。
请根据以上信息回答下列问题:
(1)写出下列物质的化学式:
B 、 C 、乙
(2)写出反应①的离子反应方程式:
(3)写出反应⑤的离子反应方程式:
19.(12分)
已除去泥沙的粗盐中,仍含有Mg2+、Ca2+和SO42-,请填写下列空格,完成将粗盐提纯,得到氯化钠晶体的实验设计。
实验目的:粗盐提纯,得到纯净氯化钠晶体
实验用品:(1)药品:粗盐、NaOH溶液、HCl溶液、Na2CO3溶液、BaCl2溶液、pH试纸、蒸馏水 (2)仪器(略)
填写下表中所缺实验步骤和操作过程:
|
序 号 |
实验步骤 |
简述实验操作 (不必叙述如何组装实验装置) |
|
① |
|
将粗盐放入烧杯中,加入适时的蒸馏水,充分搅拌,直至固体全部消失 |
|
② |
加入NaOH溶液 |
逐滴加入氢氧化钠溶液,直至不再出现沉淀为止 |
|
③ |
加入 |
逐滴加入该溶液,直至不再出现沉淀为止 |
|
④ |
加入 |
逐滴加入该溶液,直至不再出现沉淀为止 |
|
⑤ |
过滤 |
安装好过滤器,将④烧杯中的悬浊液沿玻璃棒加入过滤器中过滤 |
|
⑥ |
滴加盐酸 |
向滤液中逐滴加入盐酸,并用pH试纸检测溶液,至溶液呈中性 |
|
⑦ |
|
|
实验问题讨论:
(1)甲同学在多次过滤后,发现烧杯中的滤液仍浑浊。分析他操作不当的原因可能是 ________________________________________________________________ ;
(2)乙同学过滤后,滤液是澄清的,当取少量蒸发后的氯化钠晶体,溶于水,滴加硫酸钠溶液时,却出现白色沉淀。分析乙在实验过程中存在的问题可能是
___________________________ __________________________________________________________________。
(3)实验室进行NaCl溶液蒸发时,一般有以下操作过程:①放置酒精灯②固定铁圈的位置③放上蒸发皿④加热搅拌⑤停止加热、余热蒸干。其正确的操作顺序是 。
A.①②③④ B.①②③④⑤ C.②③①④⑤ D.②①③④⑤
18.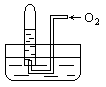 如图所示,试管中盛装的是红棕色气体(可能是混合物),当倒扣在盛有水的水槽中时,试管内水面上升,但不能充满试管,当向试管内鼓入氧气后,可以观察到试管中水柱继续上升,经过多次重复后,试管内完全被水充满,原来试管中盛装的可能是什么气体
如图所示,试管中盛装的是红棕色气体(可能是混合物),当倒扣在盛有水的水槽中时,试管内水面上升,但不能充满试管,当向试管内鼓入氧气后,可以观察到试管中水柱继续上升,经过多次重复后,试管内完全被水充满,原来试管中盛装的可能是什么气体
A.可能是N2与NO2的混和气体 B.可能是O2与NO2的混和气体
C.可能是NO与NO2的混和气体 D.只能是NO2一种气体
第Ⅱ卷(非选择题共46分)
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com