
题目列表(包括答案和解析)
3.我国的“神州七号”载人飞船已发射成功,我国探月工程计划的一个重要目的是开发月球
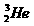
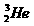
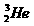 新能源 ,10t 就能满足我国一年所有能源需求。下列关于 说法正确的是
新能源 ,10t 就能满足我国一年所有能源需求。下列关于 说法正确的是
A、质量数为3,电子数为3 B、质子数为2,电子数为2
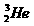
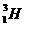 C、 与 互为同位素 D、质量数为3,中子数为2
C、 与 互为同位素 D、质量数为3,中子数为2
2.根据浙江中心气象台报道,近年每到春季,我省沿海一些城市多次出现大雾天气,致使
高速公路关闭,航班停飞。雾属于下列分散系中的 ( )
A、溶液 B、悬浊液 C、乳浊液 D、胶体
1.“中国”的英文单词叫China,这是由于中国制造的某种物质驰名世界,这种物质是( )
A、瓷器 B、铜鼎 C、钢铁 D、铝制品
28.在某100 ml混合液中,HNO3和H2SO4的物质的量浓度分别是0.4 mol·L-1、0.1mol·L-1,向该混合液中加入1.92克Cu 粉,待充分反应后,所得溶液中的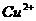 的物质的量浓度是多少?
的物质的量浓度是多少?
计算过程:
鞍山市第十三中学
2008-2009学年度第一学期 期末考试
|
27.向含有1mol KAl(SO4)2的溶液中加入Ba(OH)2溶液,使SO42-恰好完全沉淀,此时A1(OH)3的物质的量为______,上述过程的离子方程式为
_____________________________ __________________
26.A、B、C、D、E五种物质之间有如图所示的转化关系。物质A为固体; E的浓溶液常温下为粘稠态,且具有强氧化性。
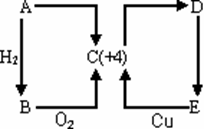 (1)请写出以上五种物质的化学式:
(1)请写出以上五种物质的化学式:
|
 A______;B______;C______;D______;E_____
A______;B______;C______;D______;E_____
(2)常见的:①温泉水、②煤、③药皂、④火药、⑤石油、⑥火柴、⑦化学肥料、⑧天然气
这些物质中,含有A的有 (填序号)。
(3)刚刚制成的湿粉丝,常挂在房中用C来熏制,利用了C的 性;实验室中可用_____ (填试剂)来检验的C存在。
25.黄铜矿(CuFeS2)是制取铜及其化合物的主要原料之一,还可以制备硫及铁的化合物。
I 冶炼铜的反应为
8CuFeS2+21O2 8Cu+4FeO+2Fe2O3+16SO2
8Cu+4FeO+2Fe2O3+16SO2
若CuFeS2中Fe的化合价为+2,反应中被还原的元素是 (填元素符号)
II上述冶炼过程产生大量SO2。下列处理方案中合理的是 (填代号)
a.高空排放
b.用于制备硫酸
c.用纯碱溶液吸收制Na2SO4
d.用浓硫酸吸收
III 利用黄铜矿冶炼铜产生的炉渣(含Fe2O3、FeO、SiO2、Al2O3)可制备Fe2O3。方法为
用稀盐酸浸取炉渣,过滤,涉及的离子方程式为(可填满也可不填满)
_____________________________________________________
_____________________________________________________
_____________________________________________________
_____________________________________________________
②滤液先氧化,再加入过量NaOH溶液,过滤,将沉淀洗涤、干燥、煅烧得Fe2O3。
a.除去Al3+的离子方程式是
b.选用提供的试剂,设计实验验证炉渣中含有FeO
提供的试剂:
稀盐酸、稀硫酸、KSCN溶液、KMnO4溶液、NaOH溶液、碘水
所选试剂为
证明炉渣中含有FeO的实验现象为
_________________________________________________________
③ Fe2O3俗称__________ ,写出它的一种工业用途
24.胃酸过多是常见的胃病,以下叙述分别是两种常见胃药的说明摘要。
甲:(1)白色结晶状粉末,可缓缓分解;(2)能溶于水,水溶液呈弱碱性;
(3)遇酸及酸性药物则产生二氧化碳。
(4)胃酸过多患者服用后多见胃胀气,甚至有引起溃疡穿孔的危险。
乙:(1)与胃酸的中和作用缓慢而持久,可维持3-4小时。(2)凝胶本
身覆盖于溃疡面上,具有保护作用。(3)可溶于稀酸或氢氧化钠溶液中。
(1)请你推测,甲中含有的主要化学成分是__________(填化学式);
乙中含有的主要化学成分是___________(填化学式)。
(2)试写出甲中含有的主要化学成分引起胃胀气反应的离子方程式:
_______________________________ _____。四、实验题(共14分)
22.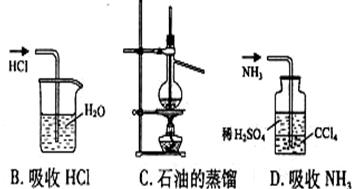 用下列实验装置完成对应的实验(部分仪器巳省略),能达到实验目的的是
( )
用下列实验装置完成对应的实验(部分仪器巳省略),能达到实验目的的是
( )
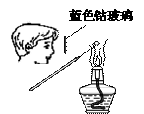
A.检验K2CO3中的K+
23工业上拟用铜和硝酸来制备Cu(NO3)2· 3H2O,下面有三位同学提出了不同
的生产方案:
甲方案:Cu+浓HNO3→ 蒸发结晶
乙方案: Cu+稀HNO3→ 蒸发结晶
丙方案:Cu+O2→CuO+稀HNO3蒸发结晶
你认为______方案最好,
理由___________ ____________________ _________
21.右图装置可用于( )
A.除去碳酸氢钠固体中的碳酸钠
B.铜与浓硝酸反应制取二氧化氮气体
C.加热铵盐和碱的混合物制取氨气
D.加热氯化铵制取氨气
涉及到的化学方程式为:_______________________________
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com