
题目列表(包括答案和解析)
2.下列有关实验操作不正确的是
A.过滤时漏斗中的液体只要不超过漏斗口即可
B.做焰色反应时铂丝应用稀盐酸洗净,并灼烧至与原火焰颜色一致
C.NaCl溶液蒸发结晶时,应将蒸发皿中NaCl 溶液全部加热蒸干
D.萃取操作时,应选择有机萃取剂,且萃取剂的密度必须比水大
1.下列物质中含氧原子数最多的是( )
A.0.2molCO2 B.标况下4.48L的CO气体
C.9.03×1022个SO2分子 D.10g的CaCO3固体
22.(10分)实验室用8.7g的MnO2与50ml足量的浓盐酸制取氯气
(1)写出制取氯气的反应方程式
(2)求生成氯气的体积(标准状况)
(3)若向反应后的剩余溶液中,加入足量AgNO3溶液,生成沉淀57.4g,求原浓盐酸的物质的量浓度。
21.(8分)为了探究铁与氯气的反应,某同学甲设计了如下的实验方案。
其实验装置为:
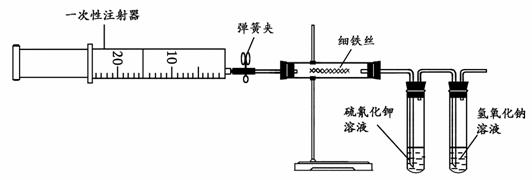
其实验步骤为:
(1)用注射器吸取20 mL左右的氯气。
(2)在硬质玻璃管内加入一定量的细铁丝,一支试管内加入硫氰化钾溶液,另一支试管中加入氢氧化钠溶液。按图所示连接实验装置,并固定在铁架台上。经检验装置不漏气。
(3)加热硬质玻璃管内铁丝约1 min,然后把注射器中的氯气注入到硬质玻璃管内,观察实验现象。硬质玻璃管中可观察到的主要现象是 ______________ ____________________________ 。A中可观察的主要现象是 __________ _ _。
(4)请写出试管B中氢氧化钠溶液的作用是 。
B中所发生反应的离子方程式为 。
20.(8分)实验室配制500 mL 0.5 mol·L-1的NaCl溶液,有如下操作步骤:①把称量好的NaCl晶体放入小烧杯中,加适量蒸馏水溶解;②把①所得溶液小心转入500mL容量瓶中;③继续向容量瓶中加蒸馏水至液面距离刻度2-3厘米处,改用胶头滴管小心滴加蒸馏水至溶液凹液面底部,与刻度线相切;④用少量蒸馏水洗涤烧杯和玻璃棒2-3次,每次洗涤的液体都小心转入容量瓶,并轻轻摇匀;⑤将容量瓶塞紧,充分摇匀。
请填写下列空白:
(1)实验操作步骤的正确顺序为(填序号) 。
(2)若出现如下情况,对所配溶液浓度将有何影响?没有进行操作④ (偏高,偏低或不变)。
(3)若实验过程中出现如下情况如何处理?加蒸馏水时不慎超过了刻度 ;向容量瓶中转移溶液时(实验步骤②)不慎有液滴掉在容量瓶外面 。
19.(10分) A是一种红棕色金属氧化物,B、D是金属单质,J是一种难溶于水的白色化合物,受热后容易发生分解。
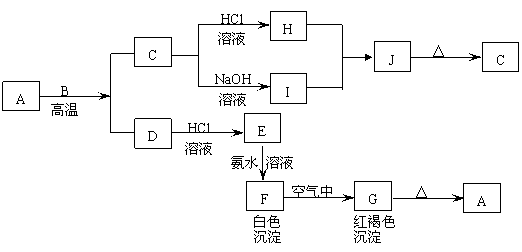
(1)写出下列物质的化学式:
A: E: J: G:
(2)按要求写方程式:
A与B在高温条件下生成C和D的化学方程式:
F在空气中转化为G的化学方程式:
C转化为I的离子方程式:
18.(10分)氧化还原反应在工农业生产和日常生活中有广泛运用
(1)人通过呼吸作用吸入氧气,氧化体内的葡萄糖(C6H12O6)提供能量以维持生命活动,反应为:C6H12O6+6O2→6CO2+6H2O+能量,该反应中的还原剂是 。
(2)罐头厂在装食物罐头时,通常要添加一些对人体无害的防腐剂,防止食物被空气中的氧气氧化而变质。此类食物防腐剂应具有 。 (填“氧化性”或“还原性”);
(3)铁是生物体中不可缺少的微量元素,铁在人体中是以Fe2+和Fe3+的形式存在的,而 Fe2+更容易被吸收。服用维生素C可使食物中的Fe3+转化为Fe2+。在这个过程中维生素C所起的作用是 。(填“氧化作用”或“还原作用”);
(4)缺铁性贫血患者应补充Fe2+,通常以硫酸亚铁的形式,而硫酸铁则无这种药效。当用硫酸亚铁制成药片时外表包有一层特殊的糖衣,这层糖衣的作用是 。
(5)Fe3+在工业上有重要用途。例如印刷电路板是由高分子材料和铜箔复合而成,可用FeCl3溶液作“腐蚀剂”刻制印刷电路,生成CuCl2和FeCl2,写出离子方程式
___________ 。
17.(6分)(1) 0.5mol H2O的质量为_______________,其中含有_______________个水分子,__________________个电子。
16.把含有氧化铁的铁片投入到足量的稀硫酸中,直到铁片完全溶解,经分析该溶液中无Fe3+,且生成的Fe2+与反应生成的H2的物质的量之比为3︰1,则原混合物中Fe2O3与Fe的物质的量之比为
A.1︰1 B.2︰5 C.4︰1 D.3︰1
选择题答题表
第II卷(共52分)
15.下列各组中的离子,能在溶液中大量共存的是
A、 H+ Na+ CO32- Cl- B、 Ba2+ Na+ Cl- SO42-
C、 K+ H+ SO42- OH- D、 Ag+ Al3+ NO3- H+
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com