
题目列表(包括答案和解析)
4.下列叙述正确的是 ( )
A.含金属元素的离子一定是阳离子
B.金属阳离子被还原不一定得到金属单质
C.强电解质溶液导电性一定强
D.在氧化还原反应中,非金属只做氧化剂
3.下列电离方程式错误的是 ( )
①NaHCO3 ====Na++H++CO32- ②NaHSO4====Na++H++SO42-
③H2SO4====2H++SO42- ④KClO3====K++Cl-+3O2-
A.①② B.① C.③④ D.①④
2.下列各组物质,前者属于电解质,后者属于非电解质的是 ( )
A.NaCl晶体、BaSO4 B.铜、二氧化硫
C.液态的醋酸、酒精 D.熔融的KNO3、硫酸溶液
1. 苹果汁中含有Fe2+,它是人们喜欢的一种补铁饮料,现榨的苹果汁在空气中会由淡绿色逐渐变为棕黄色。若榨汁时加入维生素C,可以防止这种现象发生。这说明维生素C具有 ( )
A.还原性 B.氧化性 C.碱性 D.酸性
33.(10分)(1)实验室常用的浓盐酸密度为1.17g·mL-、质量分数为36.5%。此浓盐酸的物质的量浓度为 mol·L-。若将此浓盐酸42.8mL用蒸馏水稀释至200mL,稀盐酸的物质的量浓度为 mol·L-。
(2)已知:2KMnO4+16HCl(浓)=2KCl+2MnCl2+5Cl2↑+8H2O,此反应不需要加热,而且对盐酸的浓度要求不高。当15.8g高锰酸钾参加反应时,在标准状况下生成的氯气的体积为多少?(写出计算过程,保留相应的有效数字)
(3)如果将(2)中所得氯气全部用于制取漂白粉,求:理论上可制得的次氯酸钙的质量。(写出有关反应的化学方程式及计算过程,保留相应的有效数字)
附加题:(10分,12班加考试题,其他班不计入总分。请将答案另外一张答题纸上)
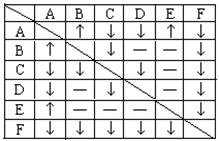 有A、B、C、D、E、F六瓶未知溶液。它们
有A、B、C、D、E、F六瓶未知溶液。它们
是MgSO4、BaCl2、(NH4)2CO3、AgNO3、HBr和
NaOH。为了鉴别,各取少许溶液进行两两混合试
 验,结果如右表。表中“¯”表示有沉淀或生成微溶
验,结果如右表。表中“¯”表示有沉淀或生成微溶
化合物,“”表示有气体生成,“-”表示观察不到
明显的现象变化。由此可以判断:
(1)A是 ,E是 ,
F是 。
(2)写出 反应的化学方程式:
B与C 。
C与D 。
福州三中08-09学年上学期期中测试卷
32.
 (10分)海水占地球总储水量的97.2%。若把海水淡化和化工生产结合起来,既可以解决淡水资源缺乏的问题,又可以充分利用海洋资源。
(10分)海水占地球总储水量的97.2%。若把海水淡化和化工生产结合起来,既可以解决淡水资源缺乏的问题,又可以充分利用海洋资源。
(1)海水中含有大量的氯化钠。请写出氯原子的原子结构示意图 。
(2)目前国际上实用的“海水淡化”主要技术之一是蒸馏法。蒸馏法是将海水变成蒸汽,蒸汽经过冷却而得高纯度淡水,由此可判断蒸馏法是 (填物理变化、化学变化)
(3)工业上利用电解饱和食盐水可制得重要化工产品,又称为“氯碱工业”。电解饱和食盐水的化学方程式为 。利用电解所得气体制36.5%的浓盐酸100t,最少需要消耗食盐 t。
(4)近年来有人提出了一种利用氯碱工业产品及氯化钠循环治理含二氧化硫废气并回收二氧化硫的方法,该方法的流程如下:
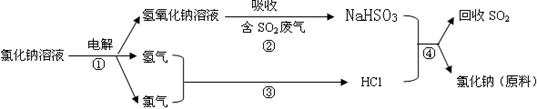
已知二氧化硫SO2是一种酸性氧化物。写出②④的化学反应方程式:
②
④
31.(15分)(1)2003年4月重庆市天原化工总厂发生了严重的氯气汇漏和爆炸事故,在此次事故中有9人死亡,3人受伤,15万人紧急疏散。根据你所学知识回答下列问题:
氯气是一种 气体(填颜色),有强烈的刺激性气味,氯气发生泄漏后政府立即组织周围的群众紧急疏散,这是由于氯气 。事故发生后消防官兵迅速赶到现场,不断地向漏气罐周围喷射水幕,这样做的目的是
(用化学方程式表示)。假设你当时在事故现场,你应该如何自救,保护自己 。
(2)下图是实验室制取氯气和检验氯气性质的装置,简答下列问题:
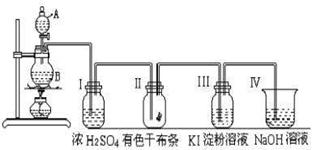
① 瓶I中浓硫酸的作用 。 ② 瓶II中干有色布条 (填现象),因为 。 ③ 瓶III中KI淀粉溶液 (填现象)。
④ 烧杯Ⅳ中,NaOH溶液的作用是 ,有关反应的化学方程式为 。
⑤ 装置中A仪器的名称是 。如果在该装置的基础上添加一些仪器以收集氯气,你认为可以选择的收集方法是 (任写一种)。
30.(10分)对一份白色固体,经过初步分析得知,其含有NH4NO3、Na2CO3、Na2SO4、NaCl、CuSO4等物质中的一种或几种。甲乙两位同学为了进一步确定这份白色固体的组成成份而进行了如下实验,但实验中的有些问题还需你来作答。
(1)甲同学取少量白色固体在试管内用水溶解,结果得无色澄清的液体。因此,甲同学说肯定有一种物质不存在。这种物质的化学式是______________
(2)甲同学又先后向那试管内依次加入了稍过量的BaCl2溶液和稀硝酸,结果是先产生了白色沉淀,后又有一部分沉淀消失并从溶液里冒出无色气泡。因此甲同学又说肯定有两种物质存在。这两种物质是:______________、_____________ 。
(3)乙同学将甲同学所得混合物进行了过滤,取滤液约2mL盛于另一支洁净的试管里,然后又向该试管内加入了稍过量的AgNO3溶液和稀硝酸,结果也产生了白色沉淀。因此乙同学说那份白色固体中也肯定有NaCl。你认为乙同学的结论(填“对”或“不对”) ,理由是 。
(4)乙同学欲鉴定甲同学实验所得滤液中是否有NH4NO3,你认为他至少应该选择的实验用品是 ,有关反应的化学方程式为 。
29.(7分)今欲用NaOH晶体配制450mL 0.800mol/L的NaOH溶液。根据题意填空:
(1)配制该溶液应选用的容量瓶标有的三个参数是 。
(2)用托盘天平称取 g固体NaOH。
 (3)向装有称好的NaOH固体的500mL大烧杯中倒入约200mL蒸馏水,用
搅拌至完全溶解。待
后,将烧杯中的溶液用玻璃棒引流转移至容量瓶
(3)向装有称好的NaOH固体的500mL大烧杯中倒入约200mL蒸馏水,用
搅拌至完全溶解。待
后,将烧杯中的溶液用玻璃棒引流转移至容量瓶
(4)用少量蒸馏水洗涤烧杯 次,洗涤液 轻轻晃动容量瓶,使溶液混和均匀。
(5)向容量瓶中加入蒸馏水到液面离刻度线1-2cm处时,改用 加蒸馏水至液面与刻度线相切。盖好瓶塞, 。将配制好的溶液转移到试剂瓶,贴好标签。
28.(5分)选择下列实验方法分离物质,将分离方法的序号填在横线上。
A、萃取分液法 B、加热分解 C、结晶法 D、分液法 E、蒸馏法 F、过滤法
(1) 分离饱和食盐水和沙子的混合物。
(2) 从硝酸钾和氯化钠的混合溶液中获得硝酸钾。
(3) 分离水和汽油的混合物。
(4) 分离四氯化碳(沸点76.75°C)和甲苯(沸点110.6°C),(已知二者互溶)。
(5) 提取溴水中的溴单质。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com