
题目列表(包括答案和解析)
2.设阿伏加德罗常数(NA)的数值为nA,下列说法正确的是
A.1molCl2与足量Fe反应,转移的电子数为3nA
B.23g钠在氧气中完全燃烧失去电子数为0.5 nA
C.常温常压下,46 g的NO2和N2O4混合气体含有的原子数为3nA
D.0.10mol Fe粉与足量水蒸气反应生成的H2分子数为0.10nA
1.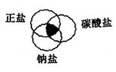 符合右图中阴影部分的物质是
符合右图中阴影部分的物质是
A.Na2CO3 B.Cu2(OH)2CO3
C.NaCl D.NaHCO3
24.(6分) 向50 mL浓度为18.4 mol·L-1的浓硫酸中加入过量的锌使H2SO4全部反应,生成标准状况下的气体16.8L。计算:
(1)反应中消耗的锌的质量;
(2)反应中生成的氢气的物质的量。
23.(6分)2.4 g 镁与100 mL稀硫酸完全反应,反应前后溶液体积的变化忽略不计。
求:(1)产生的气体在标准状况下的体积。
(2)反应完全后,所得溶液中镁离子的物质的量浓度。
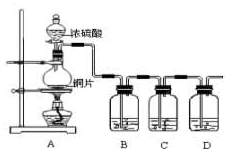
22.( 6分)某化学兴趣小组的同学为探究二氧化硫的化学性质,设计了如下图所示的装置。
请回答下列问题。
(1)铜和浓硫酸反应的化学方程式为 。
(2)B瓶中盛有品红溶液,观察到品红溶液褪色,这是因为 SO2具有 (填选项的字母,下同),C瓶中盛有新制的氯水,观察到氯水褪色,这是因为SO2具有 。
A.氧化性 B.还原性 C.漂白性
(3)D瓶中盛有NaOH溶液,作用是 。
(4)充分反应后,小组同学发现铜和硫酸都有剩余。若想使剩余的铜片溶解,可再加入
(填选项的字母)。
A.HNO3 B.NaNO3 C.NaHCO3 D.Na2CO3
四 计算题 (12分)
21.( 6分) (1)配制500mL 2.5mol/L浓度的NaOH溶液时,需要的玻璃仪器,除了烧杯、玻璃棒外,还必须有的是 、 。
⑵ 现有一瓶A和B的混合液,已知它们的性质如下表
|
物质 |
熔点/oC |
沸点/oC |
密度/g·cm-3 |
溶解性 |
|
A |
-11.5 |
198 |
1.11 |
A、B互溶,且均易溶于水 |
|
B |
17.9 |
290 |
1.26 |
 据此分析,将A和B相互分离的常用方法是:
。
据此分析,将A和B相互分离的常用方法是:
。
20.(5分)某银白色固体A放在空气中可氧化成白色固体B;将A点燃,火焰呈黄色,生成浅黄色固体C;A、B、C均可跟无色液体D反应,生成碱性物质E;其中A跟D反应时还可生成可燃性气体F,C跟D反应时则可生成另一种气体G;F和G混合后遇火可剧烈反应而发生爆炸并生成D。
(1).写出下列物质的化学式:C: ,D: ,E: ,G: 。
(2).写出A与D反应的化学方程式:
三 实验题 (12分)
19.(4分) 工业上用电解饱和食盐水的方法生产氯气和烧碱。
(1)2004年4月15日,某化工厂发生氯气泄漏事件,工作人员喷射NaOH溶液形成液幕,包围并吸收泄漏的氯气,其反应原理为 (用离子方程式表示)。
(2)事件过后,附近居民向记者反映当时晾在外面的衣服褪色了,其原因是
(结合化学方程式解释)。
18.( 共15分 其中第一空1分 ,其余每空2分 )回答下列问题:
(1)除去铁粉中混有的铝粉可以选用的试剂为 (填序号)。
A.稀盐酸 B.氢氧化钠溶液 C.浓硫酸
涉及反应的离子方程式为 。
(2)为了检验某未知溶液是否是FeCl2溶液,一位同学设计了以下实验方案加以证明。
方案:向一支装有该未知溶液的试管中先通入氯气,再滴加KSCN溶液,溶液呈现红色,证明该未知溶液是FeCl2溶液。回答以下问题:
①你认为此方案是否合理 (填”合理”或”不合理”),若不合理,要检验Fe2+应如何操作 (若填”合理”,则此空可不答)
(3) 现向一支装有FeCl2溶液的试管中滴加氢氧化钠溶液,可观察到的现象是 ,有关的化学方程为 , 。
(4)实验室在保存FeCl2溶液时为了防止FeCl2溶液变质,经常向其中加入铁粉,其原因是(用离子方程式表示) 。
17.(4分) 在标准状况下,将 L NH3溶于水得到0.5 mol·L-1的氨水500 mL;
配制100 mL 0.1 mol·L-1CuSO4溶液,需要CuSO4·5H2O g。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com