
题目列表(包括答案和解析)
18.(8分)下图为一些常见物质的转化关系图(部分反应物与生成物未标出)。A、H为单质,其中H为气体;B、E为无色液体,F为淡黄色固体,K为红褐色固体;D的大量排放是形成酸雨的重要原因。
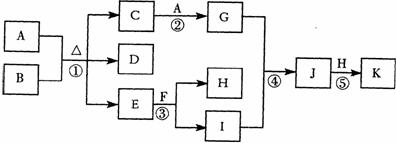
回答下列问题:
(l)在常温下,A和B发生的变化称为 。
(2)实验室制取F的方法是 。
(3)向C溶液中通入D,也能实现C→G的转化,则该反应的离子方程式是 。
(4)反应⑤化学方程式是
17.(12分)某课外活动小组用如图所示的实验装置探究氯气与氨气之间的反应。其中A、F为氯气和氨气的发生装置,D为纯净、干燥的氯气与氨气反应的装置。
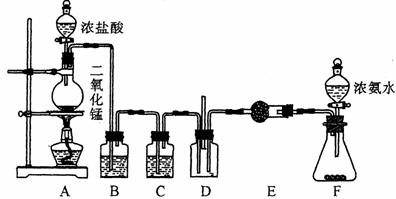
请回答下列问题:
(1)实验室用二氧化锰和浓盐酸反应制取氯气,同时生成二氯化锰和水,写出该反应的化学方程式并用单线桥标出电子转移的方向和数目。
(2)洗气瓶B的作用是 。c、E都是干燥装置,其中E中干燥管内所装的试剂是
(3)反应开始后装置D中出现浓厚的白烟并在容器内壁凝结,活动小组拟继续通过实验鉴定该固体的成分。请你协助他们完成该实验探究。
步骤①:取固体样品加少量水溶解,分装于两支试管中。向其中一支试管中加入浓NaOH溶液,加热,将湿润的红色石蕊试纸放在试管口附近,红色石蕊试纸变蓝,证明该固体中含有
步骤②:
(4)从绿色化学的角度考虑该装置中有一明显不合理之处,请你提出改进的意见。
16.(8分)海带含有丰富的碘,为了从海带中提取碘,某研究性学习小组设计并进行了以下实验:
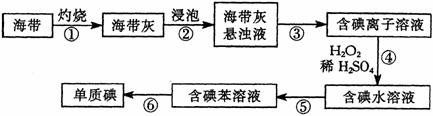
请填写下列空白:
(1)步骤⑤的实验操作名称是 。
(2)步骤⑥的目的是从含碘苯溶液中分离出单质碘和回收苯,该步骤应选择的实验装置是 。
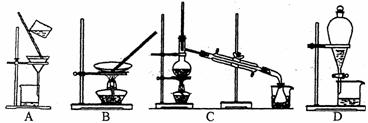
(3)步骤④反应的离子方程式是 。
(4)请设计一个简单的实验方案,检验提取碘后的水溶液中是否还含有单质碘: 。
14.某溶液中含有大量的下列离子:Fe3+、SO42-、A13+和M离子,经测定Fe3+、SO42-、A13+和M离子的物质的量之比为2:4:1:1,则M离子可能是下列中的
A.Na+ B.OH- C.S2- D.C1-
|
分内容。据此下列说法正确的是
A.该硫酸试剂的物质的量浓度为18.4mol·L-1
B.该硫酸与等体积的水混合所得溶液的质量分数小于49%
C.配制200.0mL 4.6mol·L-1的稀硫酸需取该硫酸50.0mL
D.2.7gAl与足量的该硫酸反应可得到标准状况下的H2 3.36L
第二卷(非选择题共50分)
13.下列反应的离子方程式书写正确的是
A.氯气和水的反应:C12+H2O=2H++C1-+ClO-
B.向A12(SO4)3溶液中加入过量的氨水:A13++3NH3·H2O=A1(OH)3↓+3NH4+
C.FeCl2溶液中通入C12:Fe2++C12=Fe3++2C1-
D.铜片加入稀硝酸中:3Cu+2NO3-+8H+=3Cu2++2NO↑+4H2O
12.用NA 表示阿伏加德罗常数的值,下列说法中正确的是
A.标准状况下,22.4LCO2气体中含氧原子数目为2NA
B.1mo1·L-1的A1C13溶液中,C1-离子的数目为3 NA
C.任何条件下,23gNa+离子含有的最外层电子数为NA
D.60g的二氧化硅可与水反应生成硅酸的分子数为NA A
11.在使用容量瓶配制溶液时,下列操作不正确的是
A.使用容量瓶前都必须检查容量瓶是否漏水
B.容量瓶用蒸馏水洗净后,再用待配溶液润洗
C.称好的固体试样需用纸条小心地送入容量瓶中
D.摇匀后发现凹液面下降,不加水至刻度线
10.在一定温度下,1 mol金属铜与足量某浓度的硝酸完全反应,生成NO2和NO的物质的量之比为1:3,则反应过程中转移的电子总数为
A.2 mol B.3 mol C.4mol D.5 mo1
9.下列实验方法不正确的是
A.用丁达尔现象鉴别颜色相似的浓溴水和Fe(OH)3胶体
B.用KMnO4溶液检验Fe2(SO4)3溶液中是否含有Fe2+
C.用等物质的量浓度盐酸可以鉴别Na2CO3和NaHCO3固体
D.用直接观察溶液灼烧的焰色可证明溶液中是否只含有Na+
8.下图为含有同一种元素的a、b、c、d四种物质的转化关系。其中a是单质,b、c是氧化物,d是酸,则a可能是①C ②N2 ③S ④F2中的

A.①和③ B.只有④ C.①②③ D.①②③④
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com