
题目列表(包括答案和解析)
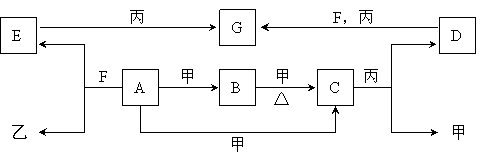
24、(16分)A、B、C、D、E、F、G为常见物质,其中C为淡黄色固体。甲、乙、丙为常见气体。各物质的转化关系如下图所示。

 回答下列问题:
回答下列问题:
(1)C的名称是 ;F的化学式 ;
A+甲→C的反应条件是 。
(2)在一定条件下,甲+乙→F,该反应属于 。
①氧化还原反应 ②非氧化还原反应 ③化合反应 ④分解反应
⑤复分解反应 ⑥置换反应 ⑦离子反应
(3)写出下列变化的化学方程式。
① B+甲→C: 。
② E+丙→G: 。
(4)检验G中是否含有D的试剂可以是 (填序号)。
①HCl ②BaCl2 ③Ca(OH)2 ④CaCl2
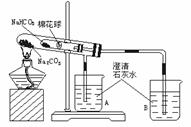
23、将HCl、H2SO4、Ba(NO3)2三种溶液,按一定顺序滴入到碳酸钠溶液中至恰好完全反应,有以下现象:
①:加入A时有白色沉淀。 ②:往①中的沉淀加入B时沉淀溶解,并有气体产生。
③:往②中的溶液中加入C时,又有白色沉淀生成。
(1)根据以上现象判断:(填化学式)A B
 (2)写出③中生成沉淀的离子方程式:
(2)写出③中生成沉淀的离子方程式:
21.(4分)下列有关实验操作或判断不正确的是 _________________(填序号,多选扣分)。
A.配制一定物质的量浓度溶液,定容时俯视刻度线会导致所配溶液浓度偏小
B.鉴定某溶液中是否含有Fe2+,取少量样品滴加少量H2O2,然后加少量KSCN溶液
C.检验某溶液中是否含有I-,可以在溶液中加淀粉溶液
D.100 mL容量瓶可用于配制95 mL 0.1 mol/L NaCl溶液
E.在天平左右两盘中各放一张白纸后,即可将NaOH固体放在白纸上称量
F.观察钾元素焰色反应的操作是:先将铂丝放在稀盐酸中洗涤,然后蘸取固体氯化钾,置于酒精灯的火焰上进行灼烧,透过蓝色钴玻璃进行观察。
G.不用任何试剂就可鉴别氯化镁、硫酸铝、硝酸铵和氢氧化钠四种无色溶液
H、鉴定某溶液是否含有Al3+可以在溶液中逐滴滴加NaOH直到过量,通过现象进行判断。
22 (1)按题意要求完成填写
①( )+( )===Fe2++H2↑ ②2OH-+( )===CO32-+H2O
③( )+3OH===Fe(OH)3↓ ④HNO3===( )+( )
⑤将HCO3-+ OH-= H2O + CO32-改写成化学方程式:__________________________________。
⑥AlO2-+H++H2O=Al(OH)3↓改写成化学方程式:______________________________________。
(2)已知某温度时发生如下三个化学反应
① C +C02=2CO:②C + H20=CO+H2 ;③ C0 +H20=CO2+H2。
由此判断,在该温度下,C、C0、H2的还原性由强到弱的顺序是________________________
(3)已知5个RO32-与2个X04-恰好完全反应,氧化产物是RO42-,则还原产物中X元素的化合价是____价。
(4)在硫酸酸化的FeSO4溶液(0.1mol/L)50mL中滴加H2O2后,溶液颜色立即有_____色变______色,
甲同学写出了该反应的离子化学方程式:aFe2++bH++cH2O2=dFe3++ eH2O,乙同学认为a=_____c ,结果
的得出应用_____________原理,丙同学认为2a+b=________d ,结果的得出应用___________原理。
而2c=e ,应用了质量守衡定律。请计算硫酸亚铁恰好反应需要0.1mol/LH2O2___________mL。
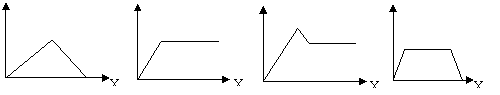
20、在硝酸铝和硝酸镁的混合溶液中,逐滴加入稀氢氧化钠溶液,直至过量。下列表示氢氧化钠加入量(X)与溶液中沉淀物的量(Y)的关系示意图中正确的是 ( )
 Y
Y
Y Y
Y
Y
Y Y
0 0 0 0
A B C D
19.甲、乙两烧杯中各盛放有100mL 3mol/L的盐酸和氢氧化钠溶液,向两烧杯中分别加入等质量的铝粉,反应结束后测得甲、乙烧杯中生成的气体在相同状况下体积比为1:2,则加入铝粉的质量为( )
A.5.4g B.3.6g C.2.7g D.1.8g
18.将过量的CO2持续通入下列八种饱和溶液:①Na2CO3 ②Na2SiO3 ③NaAlO2 ④Ca(ClO)2
⑤CaCl2 ⑥NH3和NaCl ⑦Ca(OH)2,最终能得到沉淀或析出晶体的是 ( )
A.①②③⑥ B.②⑤⑥⑦ C.①②③⑤ D.②③④
17.下列物质中既能与盐酸反应,又能与NaOH溶液反应的是 ①Na2SiO3 ②Al(OH)3 ③NaHCO3 ④Al2O3 ⑤(NH4)2CO3 A.①②④ B.②③④⑤ C.②④⑤ D.全部 ( )
16、 下列溶液中Cl-的物质的量浓度与50mL 1mol/L的AlCl3溶液中的Cl-物质的量浓度相等的是( )
A、150mL、1mol/LKCl B、75mL、2mol/LCaCl2 C、150mL、3mol/LNaCl D、75mL 2mol/L KClO3
15、 铝土矿制备铝所涉及的下列有关化学反应中,属于氧化还原反应的是 ( )
A、铝土矿溶于NaOH溶液中 B、偏铝酸钠溶液通CO2酸化 C、灼烧NaOH固体 D、电解熔融氧化铝
14、在标准状况下,含有N个氧原子的SO2的体积为a L, 则阿伏加德罗常数为 ( )
A.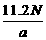 mol−1 B.
mol−1 B.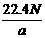 mol−1 C.
mol−1 C. mol−1
D.
mol−1
D.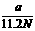 mo
mo
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com