
题目列表(包括答案和解析)
19.(10分)实验室配制500mL0.1mol/LNa2CO3溶液回答下列问题
(1)应用托盘天平称取十水碳酸钠晶体_______g
(2)若在称量样品时,药品放在天平右盘上,磕码放在天平左盘上,天平平衡时,则实际称量的碳酸钠晶体是______g(1g以下用游码)
(3)用托盘天平和小烧杯称出碳酸钠晶体的质量,其正确操作顺序的标号为_________(同一步骤可用多次)
A、调整零点
B、将游码移至刻度尺的零刻度处
C、将碳酸钠晶体放入小烧杯中称量
D、称量空的小烧杯
E、将砝码放回砝码盒内
F、记录称量结果.
(4)配制Na2CO3溶液时需用的主要仪器有____________________
(5)若实验遇下列情况,溶液的浓度是偏高,偏低还是不变?
A、加水时越过刻度线_________
B、忘记将洗涤液加入容量瓶__________
C、容量瓶内壁附有水珠而未干燥处理______
D、溶解后没有冷却便进行定容_____
18.(10分)物质有以下转化关系:
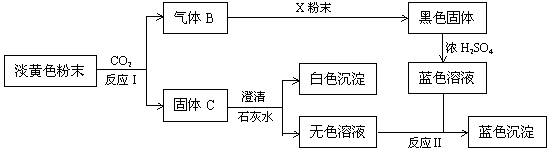
根据上图和实验现象,回答下列问题:(用化学式表示)
(1) 气体B是 ,固体C是 ,X粉末是 。
(2) 写出反应Ⅰ的化学方程式 。
(3) 写出反应Ⅱ的化学方程式 。
17.(14分)某固体混合物可能由KCl、K2SO4、KI、NaNO3、CuCl2、CaCl2和Na2CO3中的一种或几种混合而成,为鉴定其组成依次进行如下实验:
(1)混合物中加入足量水得一无色透明溶液
(2)上述溶液中滴加BaCl2有白色沉淀产生,将沉淀滤出并将滤液分成两份
(3)上述白色沉淀加盐酸时,沉淀部分溶解
(4)向一份滤液中加氯水及CCl4振荡静置CCl4层浅黄绿色
(5)往另一份滤液中加AgNO3溶液有白色沉淀产生,该沉淀不溶于HNO3
根据以上实验可判断:
①肯定存在的物质有 ,
肯定不存在的物质有 ,
可能存在的物质有 。
②写出有关反应的离子方程式:
.
16.(9分)在t℃时某NaOH饱和溶液的质量分数为a%,密度为ρg/cm3,则此饱和溶液的物质的量浓度为 ,t℃时NaOH的溶解度为 ,此溶液中Na+与H2O的个数比为 。
15.2.3 g钠投入水中,完全反应后,要使每50个水分子中含有一个钠离子,则需水量为
( )
A. 91.8 g B. 90 g C. 101.8 g D. 100 g
第Ⅱ卷(55分)
14.物质的量浓度相同的NaCl、MgCl2、AlCl3三种溶液,当溶液的体积比为3∶2∶1时,三种溶液中Cl-物质的量浓度之比为 ( )
A. 1∶1∶1 B. 1∶2∶3 C. 3∶2∶1 D. 3∶4∶3
13.设NA为阿伏加德罗常数,下列说法正确的是 ( )
A.2.3g金属钠变为钠离子时失去电子数目为0.1NA
B.32g氧气所含的原子数为NA
C.0.1mol•L-1氯化钡溶液中Cl-数目为0.2NA
D.11.2L氯气所含的原子数目为NA
12.已知反应3S+6KOH(浓) 2K2S+K2SO3+3H2O,则反应中氧化剂和还原剂的质量比是 ( )
2K2S+K2SO3+3H2O,则反应中氧化剂和还原剂的质量比是 ( )
A. 3∶1 B. 1∶3 C. 2∶1 D. 1∶2
11.下列离子方程式中正确的是 ( )
A. FeCl3溶液中通入Cl2:Fe2++Cl2=2Fe3++Cl-
B. 石灰石和稀盐酸反应:CO32-+2H=CO2↑+H2O
C. CO2通入澄清的石灰水中:CO2+2OH- =CO32-+H2O
D. NaCl溶液和AgNO3溶液混合:Ag++Cl- =AgCl↓
10.在稀溶液中能共存,加入NaOH溶液后有沉淀析出,加入盐酸后有气体逸出的一组离子是 ( )
A. Na+、SO42-、Cu2+、Cl- B. Na+、Ca2+、Cl-、HCO3-
C. K+、Na+、NO3-、CO32- D. Ca2+、K+、SO42-、CO32-
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com