
题目列表(包括答案和解析)
24.(本题共7分)
(1)过滤;玻璃棒。(2)黄(棕)色, Cl2 + 2I- == 2Cl-+ I2
(3)紫(红);萃取或分液,分液漏斗。
|
(1Al HCl FeCl3(共3分)(2)4Al+2Fe2O3 4Fe+2Al2O3(2分)
4Fe+2Al2O3(2分)
2NaCl+2H2O 2NaOH
+H2↑+Cl2↑(2分)
2NaOH
+H2↑+Cl2↑(2分)
(3)MnO2 + 4H+ + 2Cl- Mn2+ + Cl2↑+2H2O (2分) Cl2 MnO2 NaOH (共3分)
Mn2+ + Cl2↑+2H2O (2分) Cl2 MnO2 NaOH (共3分)
23.(本题共5分)
ABDEH(每选对一个得一分,每多选一个倒扣1分,最低得分为零分)
22.(本题共9分)
(1)CO2 (1分) CO2+CO32-+H2O==2HCO3-(2分)
(2)Fe (1分)Fe+2Fe3+==3Fe2+(2分)
(3)H2O(1分)3NO2+H2O==2HNO3+NO(2分)
21.(本题共12分)
(1)8∶7 2∶1 1∶1(每空2分)
(2)沸腾炉、接触室、吸收塔(3分)
(3)Fe3++3SCN-===Fe(SCN)3 (2分) 溶液呈血红色 (1分)
或者Fe3++3OH-===Fe(OH)3 出现红褐色沉淀
27.(10分)向10mLNa2CO3和Na2SO4的混合溶液中加入足量的氯化钡溶液,生成沉淀的质量为6.27g,向所得沉淀中加入足量稀盐酸,沉淀质量减少到2.33g,并放出气体,试计算:
(1)原混合物中Na2SO4的物质的量浓度;
(2)在标准状况下产生气体的体积。
评分标准
22.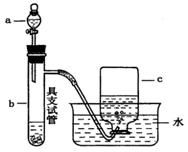 (12分)下图是探究浓、稀硝酸强氧化性的实验装置。将铜片置于具支试管的底部,在分液漏斗中加入约5mL 浓硝酸,用排水法收集产生的气体。
(12分)下图是探究浓、稀硝酸强氧化性的实验装置。将铜片置于具支试管的底部,在分液漏斗中加入约5mL 浓硝酸,用排水法收集产生的气体。
Ⅰ.探究浓硝酸的强氧化性
打开分液漏斗活塞,向具支试管中注入约3mL浓硝酸。
(1)具支试管中发生反应的化学方程式为 。
(2)实验中能证明浓硝酸具有强氧化性的现象是
、
。
Ⅱ.探究稀硝酸的强氧化性
(3)欲证明稀硝酸也具有强氧化性,紧接着向分液漏斗中加适量水稀释浓硝酸,打开活塞,注入稀硝酸。这样操作的优点是
。
(4)能证明稀硝酸与铜反应产生NO的实验现象是__________(填写序号)。
A.c中收集到无色气体;
B.c中收集到的无色气体接触空气后变为红棕色;
C.b中产生的无色气体接触空气后变为红棕色;
Ⅲ.问题讨论
在实验过程中,研究性学习小组成员观察到铜和浓硝酸反应后溶液呈绿色,当加入稀硝酸反应后溶液呈蓝色,有人认为产生这一现象的原因是由于铜离子浓度差异所引起的。请你设计一个简单实验证明这一观点是错误的。
____________________________________________________________ 。
21.(12分)A-L是中学化学中常见的物质,已知A、D是金属单质,C是一种既可溶于盐酸有可溶于氢氧化钠溶液的氧化物,G是一种黄绿色气体,H的焰色反应呈黄色。它们之间的转化关系如下图所示(部分产物已略去)。
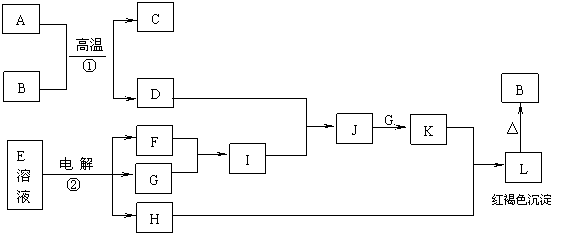
请回答:
 (1)写出物质I、K的化学式:I
,K
;
(1)写出物质I、K的化学式:I
,K
;
(2)写出反应①的化学方程式 ;
(3)写出反应②的离子方程式 ;
(4)写出C与氢氧化钠溶液反应的离子方程式 。
20.(7分)海带具有从海水中富集碘的能力,下面是从海带中提取碘单质的流程:
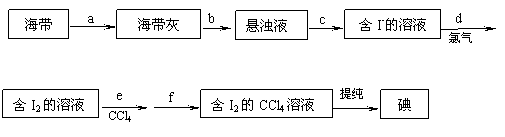

试回答:
(1)步骤a的操作名称是 ,步骤b中所加的物质是 。
(2)步骤c的操作名称是 ;该操作中涉及到的玻璃仪器有漏斗、烧杯和 。
(3)步骤d中发生反应的离子方程式为 。
(4)步骤e的操作名称是 ,操作时在含I2的溶液中加入CCl4,振荡、静置后,液体分为两层,下层液体呈 色。
(5)步骤f的操作名称是分液,所用的主要仪器是 。
19.(9分)除去下列物质中含有的杂质(括号内为杂质),请填写所需试剂的化学式及相应的反应方程式。
⑴Na2CO3溶液(NaHCO3),试剂 ;离子方程式 。
⑵FeCl2溶液(FeCl3), 试剂 ;离子方程式 。
⑶NO气体(NO2), 试剂 ;化学方程式 。
18.(12分)⑴等物质的量的O2和CO的质量比是 ,所含氧原子的个数比是 ,同温同压下的体积比是 。
⑵工业上接触法制备硫酸的主要设备有 、 、 。
⑶FeCl3溶液中滴加KSCN溶液的现象是 ,反应的离子方程式是 。
⑷实验室制取氯气的化学方程式 ;
在该反应中,氧化剂是 ,还原剂是 ;工业生产中和实验室常用 溶液吸收氯气。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com