
题目列表(包括答案和解析)
3、下列离子方程式书写正确的是
A.铝粉投入到NaOH溶液中:2Al + 2OH-══ 2AlO2-+H2↑
B.AlCl3溶液中加入足量的氨水:Al3++ 3OH- ══ Al(OH)3↓
C.三氯化铁溶液中加入铁粉:Fe3+ + Fe == 2Fe2+
D.FeCl2溶液跟Cl2反应:2Fe2++Cl2=2Fe3++2Cl-
2、某同学实际配制的NaOH溶液的浓度偏低,其原因不正确的是
A.容量瓶中原来存在少量蒸馏水 B.使用滤纸称量NaOH固体
C.溶解后的烧杯未经洗涤 D.定容时仰视刻度线
1、保护环境是每一个公民的责任,下列做法:①推广使用无磷洗涤剂;②城市生活垃圾分类处理;③推广使用一次性木质筷子;④推广使用清洁能源;⑤过量使用化肥、农药;⑥推广使用无氟冰箱。其中有利于保护环境的是
A.①②④⑤ B.②③④⑥ C.①②④⑥ D.③④⑤⑥
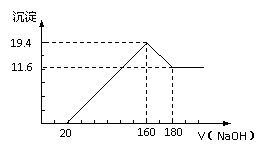
32.将一定质量的镁铝合金投入100 mL一定浓度的盐酸中,合金完全溶解。向所得溶液中滴加浓度为5 mol/L的NaOH溶液,生成的沉淀跟加入的NaOH溶液的体积关系如图。(横坐标体积单位是mL,纵坐标质量单位是g)求:
① 合金中Mg的质量
② 所用HCl的物质的量浓度
31.取11.0g氯化铵样品与足量的熟石灰混合加热,将所产生的氨气全部用1 mol/L的稀硫酸吸收,当完全吸收时,用去稀硫酸100 mL。求:
(1)样品中氯化铵的纯度。
(2)若将所产生的NH3全部溶于水配成100 mL溶液,所得氨水的物质的量浓度是多少mol/L?
30.用示意图中的简易装置可以进行气体的发生和收集。
(1)拔开试管a的橡皮塞,加入10mL6mol/L稀硝酸和1g薄铜片,立即将带有导管的橡皮塞塞紧试管口。反应开始时速度缓慢,后来逐渐加快。请写出在试管a中所发生的所有反应的化学方程式。
(2)从反应开始到反应结束,预期在试管a中可观察到哪些现象?请逐一写出。
(3)试管c收集满气体后,用拇指堵住管口,取出水槽。将管口向上,松开拇指,片刻后,再次堵住管口,将试管再倒置于水槽中,松开拇指,此时可观察到什么现象?
29.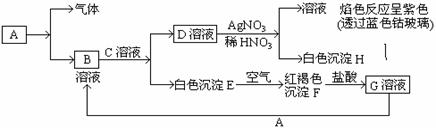 已知:以下物质能相互转化:
已知:以下物质能相互转化:
试回答:(1)写出B的化学式 ,D的化学式 。
(2)写出由E转变成F的化学方程式 。
(3)写出用KSCN鉴别G溶液的离子方程式 ;向G溶液加入A的离子反应方程式 。
28.物质A是一种高熔点化合物,不溶于强酸,但可与氢氟酸反应,A又能与纯碱在熔融时反应生成化合物B,同时放出气体C,把气体C通入B溶液中得到化合物D,将D加热又重新得到化合物A。
(1)A、B、C、D的化学式:
A ;B ;C ;D 。
(2)写出全部反应的化学方程式:
27.(1)硫酸在下列用途或反应中各表现的性质是(用字母填在横线上)。
A.难挥发性 B.强酸性 C.吸水性 D.脱水性 E.强氧化性 F.催化作用
①浓硫酸可用作气体干燥剂 ;
②往晶体硫酸铜中加浓硫酸,晶体变白 ;
③实验室制硝酸 ;(反应式为:NaNO3+H2SO4 = HNO3↑+NaHSO4)
④浓硫酸与铜反应 ;
⑤浓硫酸使润湿蓝色石蕊试纸先变红后又变黑 。
(2)运用硫酸的性质,设计实验方案鉴别两瓶等体积的硫酸,哪瓶是浓硫酸,哪瓶是稀硫酸? 。
(3)用过量的锌与浓硫酸反应时,可能产生的气体有 ,理由是
。
26.Al和Na的单质同时加入到一定量的水中,充分反应后,发现既无沉淀生成又无固体残留物存在。请用两个化学反应方程式表示其变化:
(1) ,(2) 。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com