
题目列表(包括答案和解析)
9、将100gK2CO3和KHCO3的混合物加热至质量不再变化时,共收集到CO211g,原混合物中KHCO3的质量分数是A.30% B.40% C.50% D.60% ( )
8、下列叙述正确的是
① 标准状况下,1mol任何物质的体积都约为22.4L
②常温下,2.7g铝与足量的盐酸反应,得到的电子数为0.3NA
③ 1摩尔任何物质都含有约6.02×1023个原子 ④ 64g氧气和臭氧的混合气体中含有4mol O 原子
⑤ NA个CO2的质量(以g为单位)与CO2的相对分子质量在数值上相同
⑥标准状况下,33.6LH2O含有9.03×1023个H2O分子
A、①③⑤ B、②④⑥ C、④⑤ D、④⑥
7、在下列反应中,水既不是氧化剂又不是还原剂的是 ( )
A.F2 + H2O(生成O2和HF) B.Na + H2O C.NaH + H2O(生成H2和NaOH) D.Na2O2 + H2O
5、对相同状况下的12C18O和14N2两种气体,下列说法正确的是
A.若质量相等,则质子数相等 B.若原子数相等,则中子数相等
C.若分子数相等,则体积相等 D.若体积相等,则密度相等 6、利用下列实验装置完成相应的实验,能达到实验目的的是
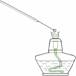
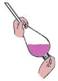

 A.检验溶液中是否含有NaCl B.除去乙醇中溶有的少量水
A.检验溶液中是否含有NaCl B.除去乙醇中溶有的少量水
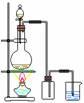
C.实验室中制取少量蒸馏水 D.用MnO2和浓盐酸制备Cl2
4、下列说法正确的是 ( )
①Na2O是碱性氧化物,可以和水反应生成相应的碱,Na2O2也可以和水反应生成相应的碱、也是碱性氧化物
②Na加入CuSO4溶液中,有红色固体生成,因为Na比Cu活泼
③自然界中不存在游离态的钠元素、氯元素 ④钠钾合金:快中子反应堆作热交换剂
⑤烧碱:治疗胃酸过多 ⑥强电解质和弱电解质的本质区别在于相同浓度时,溶液导电能力的强弱
A、①③⑤ B、②④⑥ C、②⑤ D、③④
3、判断下列有关化学基本概念的依据正确的是
A.溶液与胶体:本质不同的原因是能否发生丁达尔效应 B.纯净物与混合物:是否仅含有一种元素
C.强弱电解质:溶液的导电能力大小 D.氧化还原反应:元素化合价是否变化
2、下列反应属于氧化还原反应的是 ( )
A.2H2O2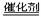 2H2O+O2↑ B.CaO+H2O=Ca(OH)2
2H2O+O2↑ B.CaO+H2O=Ca(OH)2
C.CaCO3 CaO+CO2↑ D.CaCO3+2HCl=CaCl2+CO2↑
+ H2O
CaO+CO2↑ D.CaCO3+2HCl=CaCl2+CO2↑
+ H2O
1、质检总局等6部门于2008年10月13日发出紧急通知,乳制品生产企业对在2008年9月14日以
前生产的,或未经批批检验三聚氰胺的乳制品,必须全部按照卫生部等五部门联合发布公告中三聚氰
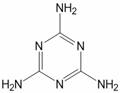
胺临时管理限量值,进行清理检查和批批检验。三聚氰胺的分子式为C3N6H6,结构如右下图所示。
下列说法不正确的是 ( )
A.三聚氰胺在生物体内主要影响泌尿系统,易产生肾结石等病症并可进一步诱发膀胱癌
 B.通知表明:2008年9月14日以前生产的乳制品一律不得再销售
B.通知表明:2008年9月14日以前生产的乳制品一律不得再销售
C.C3N6H6的摩尔质量为126g D.三聚氰胺的含氮量为66.7%
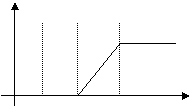
25、(12分)有50mLNaOH溶液,向其中逐渐通入一定量的CO2,随后取此溶液10mL,将其稀释至100mL,并向此稀释后的溶液中逐滴加入0.1mol/L的盐酸,产生CO2气体体积(标准状况)与所加入盐酸体积之间关系如下图所示:
 V(CO2)
V(CO2)
0 25 50 75 V(HCl)
 (甲)
(甲)
V(CO2)
0 25 50 75 V(HCl)
(乙)
试分析、计算NaOH在吸收CO2气体后,在甲、乙两种情况下,所得溶液中存在的溶质是什么?其物质的量之比是多少?且在两种情况下产生的CO2气体体积(标准状况下)各是多少?原NaOH溶液的物质的量浓度是多少?
24、(12分)常温下,在没有氧气存在时,铁与水几乎不反应,但高温下,铁能与水蒸气反
应。请设计实验,证明还原铁粉与水蒸气能够发生反应。
⑴铁粉与水蒸气反应的化学方程式是: 。
⑵证明还原铁粉与水蒸气发生了反应的方法是: 。
⑶停止反应,待装置冷却后,取出反应过的还原铁粉混合物,加入过量的稀硫酸充分反应,
过滤。简述检验所得滤液中Fe3+的操作方法:
。
⑷经检验上述滤液中不含Fe3+,这不能说明还原铁粉与水蒸气反应所得产物中不含+3价的Fe元素。原因是(结合化学方程式说明):
。
⑸某同学利用上述滤液制取白色的Fe(OH)2、沉淀,向滤液中加入NaOH溶液后,观察至生成的白色的沉淀迅速变成灰绿色,最后变成红褐色。为了得到白色的Fe(OH)2沉淀,并尽可能长时间保持其白色,可采取的措施有多种,请写出其中的两种。
第一种: 。
第二种: 。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com