
题目列表(包括答案和解析)
5.下列关于188O的叙述中,错误的是 ( )
A.质子数为8 B.中子数为8 C.电子数为8 D.质量数为18
4.下列粒子中,其最外层与最里层的电子数之和等于次外层电子数的是
A. S B.Mg C. Cl D. Be
3.美国科学家将两种元素铅和氪的原子核对撞,获得了一种质子数为118、中子数为175的超重元素,该元素原子核内的中子数和核外电子数之差为( )
A.57 B.47 C.61 D.293
2.关于原子结构的叙述正确的是 ( )
A.所有的原子核都是由质子和中子组成的
B.原子的最外层电子数不超过8个
C.稀有气体原子的最外层电子数均为8
D.原子的次外层电子数都是8
1.根据元素的核电荷数,不能确定的是 ( )
A.原子核内质子数 B.原子核中子数
C.核外的价电子数 D.原子的电子数
15.2mol·L-1解析:本题的反应式很多,有Fe2O3与H2SO4反应,生成的Fe2(SO4)3又与Fe反应,Fe与H2SO4反应;加入的NaOH与H2SO4、FeSO4反应等。但最终产物是Na2SO4和Fe(OH)2。根据守恒原理:
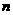 (SO
(SO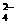 )=
)= (Na+),
(Na+),
亦即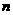 (H2SO4)=
(H2SO4)=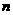 (NaOH)=
(NaOH)= 0.6mol=0.3mol。
0.6mol=0.3mol。
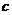 (H2SO4)=
(H2SO4)=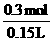 =2mol·L-l。
=2mol·L-l。
14.Zn、Cu
ZnCO3 ZnO+CO2↑
ZnO+CO2↑
C+2Cu2O 4Cu+CO2↑
4Cu+CO2↑
C+2ZnO 2Zn+CO2↑
2Zn+CO2↑
解析:我们知道,煅烧石灰石(CaCO3)能得到其氧化物,而木炭可以还原金属氧化物。把所学知识迁移过来,善于运用,不难解答。
点评:所学知识一定要灵活运用,要特别注意知识的迁移。
13.D解析:合金是两种或两种以上的金属(或金属与非金属)熔合在一起而形成的具有金属特性的物质。硬铝是由Al、Cu、Mg、Mn、Si形成的合金,黄铜是Cu-Zn合金,钢铁是Fe与其他元素形成的合金。因此唯一不属于合金的是水银。答案应为D。
点评:只要牢记并理解合金的概念,了解一些合金的名称,并能准确再现就可轻松作答。因此在学习化学的过程中,记住并理解重要的概念、原理和化学方程式,多了解一些材料是非常重要的。
12.BC解析:使澄清石灰水变浑浊的气体应为CO2,它可能是加热NaHCO3分解产生的(如C项);也可能是CO与CuO在加热条件下反应产生的:CO+CuO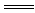 Cu+CO2(如B项)。
Cu+CO2(如B项)。
11.B解析:胃酸中含有少量盐酸,以上4种物质都能跟盐酸反应。但是,碳酸钠在反应后生成气体,造成“胀气”,而且碳酸钠碱性较强,对口腔和食道有刺激作用;氧化钙与水作用放出大量热,生成强碱,会烧伤口腔;碳酸钡溶于盐酸后生成有剧毒的氯化钡。只有氢氧化铝无副作用,对消化道无影响。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com