
题目列表(包括答案和解析)
15.配制0.25mol·L-1的NaOH溶液100mL,某学生操作如下:
①用托盘天平称出1.00g氢氧化钠:将天平调好零点,再在两盘上各取一张同样质量的纸,把游码调到1.00g的位置上,于左盘放粒状氢氧化钠至天平平衡,取下称好的氢氧化钠,并撤掉两盘上的纸。
②把称好的氢氧化钠放入一只100mL的烧杯中,加入约10mL水,搅拌使之溶解,溶解后立即用玻璃棒引流将溶液移至一只100mL的容量瓶内,加水至离刻度线约2cm处,用滴管加水至刻度线。
③写出一个标有配制日期的“0.25mol·L-1NaOH溶液”的标签,贴在容量瓶上密闭保存。指出上述操作中的7处错误:
(1)__________________________;(2)_________________________
(3)__________________________;(4)_________________________
(5)__________________________;(6)_________________________
(7)__________________________
14.下列叙述中,正确的是( )
A.在标准状况下,1mol任何物质的体积为22.4L
B.等物质的量浓度的盐酸和硫酸中,H+的物质的量浓度也相等
C.1molH2和1molHe中,所含的分子数相同、原子数相同、质量也相同
D.体积为6L的O2,其质量可能为8g
13.在4℃时向100mL水中溶解了22.4LHCl气体(标准状况下测得)后形成的溶液。下列说法中正确的是( )
A.该溶液物质的量浓度为10mol·L-1
B.该溶液物质的量浓度因溶液的密度未知而无法求得
C.该溶液中溶质的质量分数因溶液的密度未知而无法求得
D.所得溶液的体积为22.5L
12.某位同学配制一定物质的量浓度的NaOH溶液时,造成所配溶液浓度偏高的原因是( )
A.所用NaOH已经潮解
B.向容量瓶中加水未到刻度线
C.有少量NaOH溶液残留在烧杯里
D.用带游码的托盘天平称2.4gNaOH时误用了“左码右物”方法
11.如果 g某气体中含有的分子数为
g某气体中含有的分子数为 ,则
,则 g该气体在标准状况下占有的体积应表示为(式中
g该气体在标准状况下占有的体积应表示为(式中 为阿伏加德罗常数( )
为阿伏加德罗常数( )
A.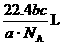 B.
B.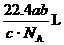
C.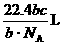 D.
D.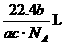
10.将标准状况下的 LHCl(g)溶于1000g水中,得到的盐酸密度为bg·cm-3,则该盐酸的物质的量浓度是( )
LHCl(g)溶于1000g水中,得到的盐酸密度为bg·cm-3,则该盐酸的物质的量浓度是( )
A.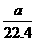 mo1·L-1 B.
mo1·L-1 B.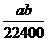 mol·L-1
mol·L-1
C.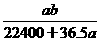 mol·L-1 D.
mol·L-1 D. mol·L-1
mol·L-1
9.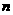 molN2和
molN2和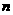 mol14CO相比较,下列叙述中正确的是( )
mol14CO相比较,下列叙述中正确的是( )
A.在同温同压下体积相等 B.在同温同压下密度相等
C.在标准状况下质量相等 D.分子数相等
8.同温同压下,等质量的SO2和CO2相比较,下列叙述中正确的是( )
A.密度比为16∶11 B.密度比为11∶16
C.体积比为16∶11 D.体积比为11∶16
7.300mL某浓度的NaOH溶液中含有60g溶质。现欲配制1mol·L-1NaOH溶液,应取原溶液与蒸馏水的体积比约为( )
A.1∶4 B.1∶5 C.2∶1 D.2∶3
6.下列数量的物质中含原子数最多的是( )
A.0.4mol氧气
B.标准状况下5.6L二氧化碳
C.4℃时5.4mL水
D.10g氖
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com