
题目列表(包括答案和解析)
22.(10分)有一包白色固体粉末,可能含有Na2SO4、CaCO3、KCl、BaCl2、CuSO4中的一种或几种,按以下步骤进行实验:
(1)将固体粉末溶于水得无色溶液和白色沉淀;
(2)加入稀盐酸,沉淀部分溶解且有气泡产生。
根据以上实验所产生的现象,判断这种混合物中,一定含有______________,一定没有______________,可能有______________。写出上述所发生反应的离子方程式___________________________、___________________________。
21.(9分)(置换题,8、9、10班做) 25℃,pH=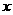 的盐酸
的盐酸 L与pH =
L与pH =  的NaOH溶液b L恰好中和(
的NaOH溶液b L恰好中和(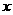 ≤6、
≤6、 ≥8)。
≥8)。
(1)若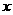 +
+ =12,则
=12,则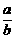 = 。
= 。
(2)若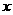 +
+ >14,则
>14,则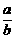 = ;(用
= ;(用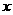 、
、 表示)且
表示)且 b(填“>”“<”或“=”)。
b(填“>”“<”或“=”)。
21.(置换题,平行班做) (12分)在下列物质中,①CaCO3(固体) ②CH3COOH(液态) ③SO2 ④ C2H5OH ⑤饱和食盐水 ⑥石墨 ⑦NaOH(固体) ⑧蔗糖 (请填写序号)
(1)能导电的是_______________________________。
(2)属于非电解质的是____________________________。
(3)属于电解质的是____________________________。
(4)属于弱电解质的是____________________________。
20.(8分)在MnO2+4HCl(浓) 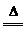 MnCl2+Cl2↑+2H2O反应中,
是氧化剂;
__________是还原剂; 被氧化; 被还原; _____是氧化产物;__________是还原产物。电子转移的总数为
e-;氧化性:MnO2 ___Cl2(填>,<或=)。
MnCl2+Cl2↑+2H2O反应中,
是氧化剂;
__________是还原剂; 被氧化; 被还原; _____是氧化产物;__________是还原产物。电子转移的总数为
e-;氧化性:MnO2 ___Cl2(填>,<或=)。
19.(8分)同温同压下,同体积的NH3和H2S气体的质量比是_________;同质量的NH3和H2S气体的体积比是________;同质量的NH3和H2S气体中所含氢原子个数比是________;若两者所含氢原子个数相等,它们的物质的量比是________。
18.将质量分数为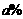 ,物质的量浓度为
,物质的量浓度为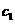
 的稀
的稀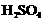 蒸发掉一定量的水,使其质量分数为
蒸发掉一定量的水,使其质量分数为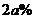 ,此时若物质的量浓度为
,此时若物质的量浓度为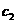
 ,则c1和c2的关系为
,则c1和c2的关系为
A.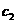 =2
=2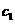
 B.
B.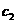 <2
<2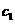 C.
C.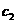 >2
>2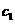 D.
D.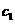 =2
=2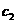

第Ⅱ卷(非选择题,共66分)
17.已知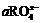 +bH++cCl-═dR2++5Cl2↑+8H2O,则
+bH++cCl-═dR2++5Cl2↑+8H2O,则 中R的化合价为
中R的化合价为
A.+4 B.+5 C.+6 D.+7
16.在标准状况下,等质量的CH4和CO2比较,下列说法中正确的是
A.密度比4∶11 B.分子数之比为4∶11
C.体积比11∶4 D.物质的量之比为4∶11
15.(置换题,8、9、10班做)20℃时,H2S的饱和溶液物质的量浓度为0.1 mol·L-1 ,其电离方程式为H2S H++HS-,HS-
H++HS-,HS- H++S2-,若要使溶液的pH增大,同时
H++S2-,若要使溶液的pH增大,同时
c(S2-)也增大,可采取的措施是
①加入适量的水 ②加入适量的Na2S固体;
③加入适量的NaOH固体 ④将溶液加热煮沸
A.①②③④ B.①② C.②③ D.③④
14.(置换题,8、9、10班做)比较1 L 0.1 mol·L-1的HCl溶液与1 L 0.1 mol·L-1的CH3COOH下列说法正确的是
A.导电能力相同 B.与锌反应开始时放出H2的速率相同
C.能中和相同物质的量的NaOH D.溶液的pH相同
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com