
题目列表(包括答案和解析)
5.下列电离方程式书写不正确的是 ( )
A.KIO3 = k+ + IO3- B.NaHSO4 = Na+ + H+ + SO42-
C.NaHCO3 = Na+ + H+ + CO32- D.CaCl2 = Ca2+ + 2Cl-
4.胶体分散系与其他分散系的本质区别是 ( )
A.是否有丁达尔现象 B.是否透明 C.分散质直径大小 D.是否稳定
3.原子结构模型的演变图中,⑴为道尔顿实心球式原子模型;⑵为卢瑟福行星运转式原子模型;⑶为汤姆生葡萄干面包式原子模型;⑷为近代量子力学原子模型;⑸为玻尔轨道式原子模型。其中符合历史演变顺序的一组排列是 ( )


A.⑴⑶⑵⑸⑷ B.⑴⑵⑶⑷⑸
C.⑴⑸⑶⑵⑷ D.⑴⑶⑸⑷⑵
2.实验室里有4个药品橱,已经存放以下物品:
|
药品橱 |
甲橱 |
乙橱 |
丙橱 |
丁橱 |
|
药品 |
盐酸,硫酸 |
氢氧化钠, 氢氧化钙 |
红磷,硫 |
铜,锌
|
实验室新购进一些碘,应该将这些碘放在 ( )
A.甲橱 B.乙橱 C.丙橱 D.丁橱
1.下图为农夫山泉矿泉水瓶上的部分说明文字,列出了该饮用天然水理化指标。
|
矿物元素
测定结果 钙 ≥4.0 mg·L-1 镁 ≥0.5 mg·L-1 钾 ≥0.35 mg·L-1 钠 ≥0.8 mg·L-1 偏硅酸 ≥1.8 mg·L-1 pH(25℃) 7.1 |
这里的钙、镁、钾、钠是指 ( )
A.元素 B.分子 C.单质 D.原子
16、(1)OH-Cl-K+(2)铁粉Ag
(3)OH-、Cl-、Ag+、Fe3+KNO3
解析:(1)甲厂的废水明显呈碱性,即含大量OH-,而Ag+、Fe3+与OH-不能共存,故Ag+、Fe3+只能在乙厂废水中,由于C1-与Ag+不共存,故Cl-在甲厂中,依电荷守恒,甲厂废水中必含的阳离子只能为K+。所以甲厂废水含OH-、C1-、K+,乙厂废水中含Ag+、Fe3+、NO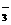 。
。
(2)加入铁粉回收银Fe+2Ag+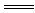 Fe2++2Ag↓
Fe2++2Ag↓
(3)混合后OH-与Fe3+、Ag+;C1-与Ag+转化为沉淀,剩下的只有KNO3。
点评:解答离子共存题,要看清题目,审准题意,挖掘出隐含条件。有的离子虽不存在于书面上的离子组中,但有时在条件中“隐含”出现,如某强酸性(或强碱性)溶液中能大量共存,说明溶液中除离子组内各离子外,还应有H+(或OH-)。此外,还要注意溶液是否有颜色。如Cu2+、Fe3+、MnO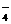 等都有颜色,若为无色则说明其不存在。
等都有颜色,若为无色则说明其不存在。
15、(1)2H++SO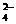 +Ba2++2OH-
+Ba2++2OH-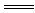 BaSO4↓+2H2O
BaSO4↓+2H2O
(2)Ba2++SO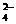
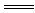 BaSO4↓
BaSO4↓
解析:因NaHSO4是二元强酸的酸式盐,可以理解成全部电离。当反应后溶液呈中性时其反应式是2NaHSO4+Ba(OH)2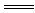 BaSO4↓+Na2SO4+2H2O,离子反应式是2H++SO
BaSO4↓+Na2SO4+2H2O,离子反应式是2H++SO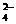 +Ba2++2OH-
+Ba2++2OH-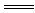 BaSO4↓+2H2O。此时中性溶液中只有Na2SO4溶液,加入B(OH)2的离子反应式为Ba2++SO
BaSO4↓+2H2O。此时中性溶液中只有Na2SO4溶液,加入B(OH)2的离子反应式为Ba2++SO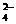
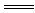 BaSO4↓。
BaSO4↓。
点评:酸式盐和碱的反应,情况比较复杂。因为由于加入碱的量不同,其产物有所不同,所以建议对此类问题先写成化学方程式再改写成离子方程式。
14、(1)K2CO3+H2SO4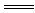 K2SO4+H2O+CO2↑
K2SO4+H2O+CO2↑
(2)AgNO3十NaCl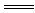 AgCl↓+NaNO3
AgCl↓+NaNO3
(3)CuSO4+2NaOH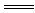 Na2SO4+Cu(OH)2↓
Na2SO4+Cu(OH)2↓
(4)SO2+2NaOH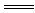 Na2SO3十H2O(或其他合理答案)
Na2SO3十H2O(或其他合理答案)
13、(1)Fe2O3+6H+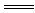 2Fe3++3H2O
2Fe3++3H2O
(2)CO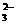 +2H+
+2H+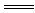 H2O十CO2↑
H2O十CO2↑
(3)Cu2++SO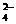 +Ba2++2OH-
+Ba2++2OH-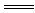 BaSO4↓+Cu(OH)2↓
BaSO4↓+Cu(OH)2↓
(4)Ca2++2OH-+CO2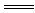 CaCO3↓+H2O
CaCO3↓+H2O
12、(1)S0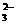 、CO
、CO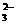
(2)SO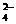 、S0
、S0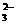 、CO
、CO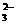
(3)Ba2+Ag
解析:当溶液中有大量H+存在时,H+与S0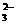 、CO
、CO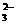 会生成气体SO2和CO2;Ba2+可以分别和SO
会生成气体SO2和CO2;Ba2+可以分别和SO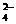 、S0
、S0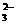 、CO
、CO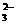 生成沉淀物;如果溶液中既含有Ba2+又含有Ag+时,上述所有阴离子都不可能存在。
生成沉淀物;如果溶液中既含有Ba2+又含有Ag+时,上述所有阴离子都不可能存在。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com