
题目列表(包括答案和解析)
6.沙子(主要成分为 )能转变成制造计算机芯片的物质硅(
)能转变成制造计算机芯片的物质硅(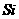 ),化学反应原理是
),化学反应原理是 高温
高温 该反应的基本类型为
该反应的基本类型为
A.化合反应 B.分解反应 C.置换反应 D.复分解反应
5.下列关于分子、原子、离子的说法正确的是
A.分子可分原子不可分 B.原子的质子数决定元素的化学性质
C.分子、原子、离子都能构成物质 D.分子由离子构成
4. 下列实验操作中,正确的是
下列实验操作中,正确的是
3.二氧化钛(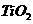 )是常用的小食品添加剂,它属于
)是常用的小食品添加剂,它属于
A.酸 B碱 C.盐 D.氧化物
2.空气的成分中,含量最多且可用于填充汽车轮胎的气体是
A.氮气 B.氧气 C.水蒸气 D.二氧化碳
1.下列变化中属于化学变化的是
A.矿石粉碎 B.酒精挥发 C.食物腐烂 D.冰雪融化
3.20℃时部分酸、碱、盐的溶解性如下表:
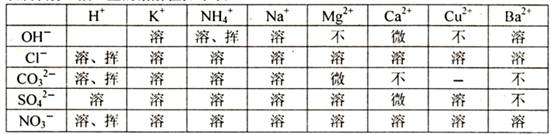 说明:表中“溶”表示那种物质可溶于水,“不”表示不溶于水,“微”表示微溶于水,“挥”表示挥发性,“一”表示不稳定或不存在。
说明:表中“溶”表示那种物质可溶于水,“不”表示不溶于水,“微”表示微溶于水,“挥”表示挥发性,“一”表示不稳定或不存在。
选择题(共10分)
注意:每小题只有1个选项符合题意:请用2B铅笔将答题卡上的相应序号涂黑。
2. 常见金属的活动性顺序如下:
常见金属的活动性顺序如下:
1.可能用到的相对原子质量:H-1 0-16 s-32 Fe-56
30.某实验小组欲用10克胆矾(CuSO4·5H2O)制取氧化铜并证明氧化铜能加快H2O2的分解。
Ⅰ.请你完成他们制取氧化铜的实验步骤。(提示:氢氧化铜受热分解生成氧化铜和水)
(1)称取10克胆矾,将其放入小烧杯中,再 ▲ 。
(2)向步骤(1)中的烧杯内滴加一定量的 ▲ 溶液,产生大量的沉淀。
(3)将步骤(2)所得混合物过滤、洗涤。
(4)检验滤液中是否含硫酸铜,操作方法是 ▲ 。
(5)检验步骤(3)固体残渣是否洗涤干净,操作方法是 ▲ 。
(6)将洗涤干净的固体残渣加热直至全部变为黑色的氧化铜。
Ⅱ.小明设计了右图实验装置来证明氧化铜能加快双氧水(溶质质量分数约5%)的分解并与二氧化锰的催化效果进行比较(即比较反应速率)。用图示装置测量产生气体的体积,其它可能影响实验因素均已忽略,相关数据如下:
|
序号 |
双氧水体积 |
催化剂 |
待测数据 |
|
① |
15mL |
无 |
|
|
② |
15mL |
CuO(0.5g) |
|
|
③ |
15mL |
MnO2(0.5g) |
|
(1)从设计装置来看,有一个明显的缺陷,你认为如何纠正 ▲ 。
(2)从设计原理看,实验中的“待测数据”可以是指 ▲ 。
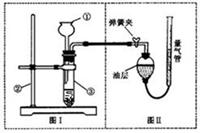 (3)实验时气体收集在图Ⅱ的球型漏斗中。若
(3)实验时气体收集在图Ⅱ的球型漏斗中。若
要保证读取的气体体积没有误差,在读数
前应进行的操作是 ▲ 。若要检验
产生的气体是氧气,应打开单孔橡皮塞,
▲ 。
(4)为探究CuO在实验②中是否起催化作用,
除与①比较外,还需补做下列实验(不必
写具体操作):a.证明CuO的化学性质没有改变;b. ▲ 。
(5)如果三个实验中所用双氧水溶质质量分数不同,对实验结果 ▲ (选填“有”或“没有”)明显影响。
Ⅲ.(1)写出双氧水在氧化铜的催化作用下分解产生氧气的方程式 ▲ 。
(2)已知该双氧水中溶质质量分数为5%,若产生氧气0.16g,那实际消耗的过氧化氢溶液质量是多少?(要有计算过程)
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com