
题目列表(包括答案和解析)
3.下列关于氧化还原反应的说法正确的是: ( )
A.得电子的物质被还原 B.还原剂具有氧化性
C.氧化剂发生氧化反应 D.作氧化剂的物质肯定不能作还原剂
2.下列状态的物质能导电,且为电解质的是
A.液态HCl B.熔融的NaCl C.铜单质 D.酒精
1.下列各类反应中,全部是氧化还原反应的是 ( )
A.分解反应 B.化合反应 C.置换反应 D.复分解反应
2321.(5分) 选择下列实验方法分离物质,将分离方法的序号填在横线上。
A、萃取分液法 B、加热分解 C、结晶法
D、分液法 E、蒸馏法 F、过滤法
(1) 分离饱和食盐水和沙子的混合物
(2) 从硝酸钾和氯化钠的混合溶液中获得硝酸钾
(3) 分离水和汽油的混合物
(4) 分离四氯化碳(沸点为76.75°C)和甲苯(沸点为110.6°C),(已知四氯化碳和甲苯互溶。)
(5) 除去氧化钙中的碳酸钙
242.(6分)在Fe3O4
+4CO 3Fe+4CO2的的中,
是氧化剂,
是还原剂,
3Fe+4CO2的的中,
是氧化剂,
是还原剂,
元素被氧化, 元素被还原,氧化产物是 ,还原产物是 。
2523.(12分)现有CO和O2两种气体
⑴当两者的质量相等时,在标准状况下:
①体积比为_________ ②密度比为________ ③分子数比为________
⑵当两者体积相同时,在相同状况下:
①质量比为_________ ②密度比为________ ③分子原子总数比为________
2624、(180分)①H2SO4的摩尔质量为
。1.204×1024个H2SO4分子物质的量为 ,其中含
molO,含H的质量为
。
(4分)② 已知2NaHCO3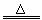 Na2CO3+H2O+CO2↑,加热10g NaHCO3一段时间后剩余固体质量为6.9g,
Na2CO3+H2O+CO2↑,加热10g NaHCO3一段时间后剩余固体质量为6.9g,
则剩余固体中含有Na2CO3的质量为 g
27 25 .
(1214分)实验室欲配制0.5mol/L的NaOH溶液500
mL。有以下仪器:
①烧杯 ②100mL量筒③1000mL容量瓶④500mL容量瓶
⑤玻璃棒⑥托盘天平(带砝码)
(1)配制时,必须使用的仪器有 (填代号),还缺少的仪器是
,该实验中两次用到玻璃棒,所起作用分别是 、 。
(2)使用容量瓶前必须进行的一步操作是 。
(3)配制时,一般可以分为以下几个步骤:①称量 ② 计算 ③溶解
④摇匀 ⑤转移 ⑥洗涤 ⑦定容 ⑧冷却,其正确的操作顺序为 。
(4)在配制过程中,其它操作都正确,下列操作会引起误差偏高的是
①未洗涤烧杯、玻璃棒 ②未等NaOH溶液冷却至室温就转移到容量瓶中③容量瓶不干燥,含有少量蒸馏水 ④定容时俯视标线⑤定容时仰视标线
四 、计算题:(5分)
28 26 (5分)将23.4gNaCl溶于水中,配成250mL溶液。计算所得溶液中溶质的物质的量浓度。
灰埠中学2008-2009学年高一年级期中考试
|
座位号 |
|
化学答题纸(重点班)
一、选择题(共14小题,每题2分,共28分,每小题只有一个选项符合题意)
二、选择题(共6小题,每题3分,共18分,每小题有一个或两个选项符合题意)
21.(5分)
(1) (2) (3) (4) (5)
22.(6分) 是氧化剂, 是还原剂, 元素被氧化, 元素被还原,氧化产物是 ,还原产物是 。
23.(12分)
⑴:①_________ ②________ ③________
⑵ ①_________ ②________ ③________
24、
(8分)① 。 , , 。
(4分)② g
27 . (14分)
(1) (填代号), , 、 。
(2) 。
(3) 。
(4)
四 、计算题:(5分)
28 (5分)
灰埠中学2008-2009学年高一年级期中考试
|
座位号 |
|
化学答题纸(重点班)
1715.某溶液中只含有Na+、Al3+、Cl-、SO42- 四种离子,已知前三种离子的个数比为3∶2∶1,则溶液中Al3+和 SO42-的离子个数比为
A.1∶2 B.1∶4 C.3∶4 D.3∶2
1816.用NA表示阿伏加德罗常数,下列叙述正确的是( )
A.标准状况下,22.4LH2O含有的分子数为1 NA
B.常温常压下,1.06g Na2CO3含有的Na+离子数为0.02 NA
C.通常状况下,1
NA 个CO2分子的质量为44g
D.物质的量浓度为0.5mol·/L的MgCl2溶液中,含有Cl- 个数为1 NA
1917. 下列有关0.1mol/LKNO3溶液的叙述正确的是( )
A、1L该溶液中含有KNO3 10.1g
B、100mL该溶液中含有NO3- 0.01mol
C、从1L该溶液中取出100mL,所取出的KNO3溶液浓度为0.1mol/L 在1L水中溶解10.1g KNO3,即可配制得0.1mol/L KNO3溶液
D、在1L水中溶解10.1g KNO3,即可配制得0.1mol/L KNO3溶液从1L该溶液中取出100mL,所取出的KNO3溶液浓度为0.1mol/L
2018. 配制0.1 mol/L的硫酸铜溶液,下列操作正确的是( )
A. 取25g 胆矾(CuSO4·5H2O)溶于1L水中
B. 取16g CuSO4 溶于水配成1L溶液.
C 取25g 胆矾溶于水配成1L溶液.
D 将胆矾加热除去结晶水,再取无水硫酸铜16 g溶于1L水中
2119、已知每个氧原子中含有8个电子,mg的氧气中含有1 mole-,则m的数值为( )
A
2
g B 4 g C
16
g D 32 g
2220、两个容积相同的容器,一个盛有一氧化氮(NO),另一个盛有氮气和氧气,在同温、同压下两容器内的气体不一定相同的是(
)
A 原子总数 B 气体物质的量 C 分子总数 D 质量
14、下列反应属于氧化还原反应的是( )
A CaCO3+2HCl====CaCl2+H2O+CO2↑
B 2NaHCO3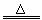 Na2CO3+H2O+CO2↑
Na2CO3+H2O+CO2↑
C Cl2+2NaOH===NaCl+NaClO+H2O
D NaBr+AgNO3===AgBr↓+NaNO3
15.下列实验操作中错误的是 ( )
A.蒸发操作时,应使混合物中的水分完全蒸干后,才能停止加热
B.蒸馏操作时,应使温度计水银球靠近蒸馏烧瓶的支管口处
C.分液操作时,分液漏斗中下层液体从下口放出,上层液体从上口倒出
D.过滤操作时,若发现滤液混浊,应重新过滤一次
16在碱性溶液中能大量共存且溶液为无色透明的离子组是
A.K+ 、MnO4-、Na+、Cl- B.K+、Na+、NO3-、CO32-
C.Na+、H+、NO3-、SO42- D.Fe3+、Na+、Cl-、SO42-
13、下列反应中,水只作为氧化剂的是( )
A.
|
C.C+H2O == CO+H2↑ D.Cl2+H2O=HCl+HClO
12、下列离子方程正确的是 ( ) B
A 氢氧化铜与稀硝酸的反应:OH- + H+=H2O
B 将金属钠加入水中:Na+2H2O==Na++2OH-+H2
C 氢氧化钡溶液与硫酸反应:SO42-+Ba2+=BaSO4↓
D 硫酸氢钠与氯化钡溶液的反应:Ba2++SO42-=BaSO4↓
11、有关电解质的说法正确的是
A.纯水的导电性很差,所以水不是电解质
B.SO3水溶液的导电性很好,所以SO3是电解质
C.液态的铜导电性很好,所以铜是电解质
D.Na2O液态时能导电,所以Na2O是电解质
10、下列溶液中Cl-物质的量浓度最大的是( )
A 100mL2mol/LMgCl2 B 1000mLl.5mol/LNaCl
C 250mLl mol/LAlCl3 D 300mL5mol/LKClO3
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com