
题目列表(包括答案和解析)
4.做焰色反应实验时所用的铂丝,每次用完后都要
A.用滤纸擦干净后才能使用
B.用水多洗几次
C.用稀盐酸洗涤后,再灼烧到无颜色时为止
D.先用稀盐酸洗涤,后用水洗涤
3.下列各种仪器:①漏斗、②容量瓶、③试管、④分液漏斗、⑤天平、⑥量筒、⑦胶头滴管、⑧蒸馏烧瓶。常用于物质分离的是
A.①③⑦ B.①④⑧ C.②⑥⑦ D.④⑥⑧
2.以下是一些常用的危险品标志,装运乙醇的包装箱应贴的图标是




A B C D
1.北京2008奥运会金牌为金镶玉,直径为70mm,厚6mm。某化学兴趣小组对金牌中金属的成分提出猜想:甲认为该金属是由纯金制成;乙认为该金属是由金银合金制成;丙认为该金属是由黄铜(铜锌合金)制成。为了验证他们的猜想,取制造这种金牌的材质粉末少量进行实验,加入下面一种试剂来证明甲、乙、丙猜想的正误,该试剂应是
A.硫酸铜溶液 B.稀硝酸 C.盐酸 D.硝酸银溶液
24、(6分)A气体极易溶于水形成A的水溶液,其相对分子质量为M,在0℃、1.01×105Pa时,测得其饱和溶液的物质的量浓度为c mol/L,该溶液的密度为d g/cm3,求:(1)A饱和溶液的质量分数;(2)0℃、1.01×105帕时,1体积水中可溶解多少体积的A气体?
23.(5分)实验室里用二氧化锰与浓盐酸反应来制取适量的氯气。现用200mL的浓盐酸与二氧化锰反应,生成的氯气在标准状况时的体积为5.6升,计算:(1)理论上需要参加反应的二氧化锰多少?(2)被氧化的HCl的物质的量为多少?
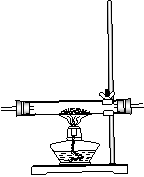
22.(12分)实验室用如图所示的仪器药品制取氯化铁粉末,已知氯化铁粉末很容易吸水生成结晶水化合物FeCl3+6H2O=FeCl3·6H2O,








 浓HCl
浓HCl
①
 A
无水CaCl2 ④⑤ ⑥ ⑦
A
无水CaCl2 ④⑤ ⑥ ⑦






 MnO2
Fe
B
MnO2
Fe
B
 ②
③
D
E
②
③
D
E

 C
C


浓H2SO4 饱和食盐水
⑴按照气体流向从左到右顺序连接仪器应是(填仪器接口顺序)
①接____,____接____,____接____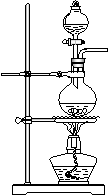
⑵烧瓶A中反应的离子方程式是 ,B中反应的化学方程式是____________
⑶容器D的作用是__________________,容器E的作用是__________________
⑷A、B中的酒精灯应先点燃 处(填“A”或“B”)的酒精灯,理由是
⑸这套实验装置是否完整? (填“是”或“否”),若不完整还须补充
装置(若第一问填“是”,则此问不需要作答)
21. (8分)根据下面物质间转换的框图,回答有关问题:
(8分)根据下面物质间转换的框图,回答有关问题:
(1)写出A、C、F物质的化学式:A ,C ,F
(2)如果1molNa2O2与足量的D物质反应,可得到标准状况下气体的体积为 L,同时反应中转移的电子总数为
NA
(3)写出焦炭(炽热)与水蒸气反应的化学方程式 ,D中混有少量B,除杂方法为
20.(8分)有一瓶澄清的无色溶液,其中可能含有K+、Na+、Cu2+、SO42-、Cl-、Br-、CO32-中的某一种或几种。取该溶液进行下列实验:
①取部分溶液加足量稀硝酸,逸出气体;
②取①逸出气体后的剩余溶液,加入足量氯水和四氯化碳,振荡后分层,油层呈棕红色;
③取②余液一部分加入BaCl2溶液有白色浑浊物产生;
④取②实验后的水层部分溶液,加入AgNO3溶液和稀硝酸有白色沉淀。试回答:
(1)原溶液中肯定存在的阴离子是 。
(2)肯定不存在的阳离子是 ,其原因是
(3)不能肯定存在与否的离子是 ,若溶液中只存在一种阳离子,要进一步确认该阳离子,操作方法是(写清具体操作过程、现象、结论):
(4)写出实验的第①②③步发生现象的反应的离子方程式:
① ② ③
19.(1)(4分)将31gNa2O溶于99g水中配成密度为d g/cm3的溶液,则此溶液的物质的量浓度为 ,此溶液中Na+与H2O的个数比为
(2)(4分)加热碳酸钠和碳酸氢钠的混合物190g,使其完全分解,得到标准状况下气体11.2升,则混合物中碳酸钠的质量分数为_______,剩余固体物质的质量为______g.
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com