
题目列表(包括答案和解析)
19.同主族元素形成的同一类型的化合物,往往结构和性质很相似,如PH4I的结构和性质与NH4Cl相似,有关对PH4I的叙述中不正确的是: ( )
A.可由PH3与HI化合生成 B.将其加热可以分解
C.能跟NaOH溶液反应 D.是一种共价化合物
18.NO和CO都是汽车尾气中的有害物质, 它们能缓慢地反应生成氮气和二氧化碳,对此反应,下列叙述正确的是( )
A.使用适当的催化剂不改变反应速率 B.降低压强能提高反应速率
C.升高温度能提高反应速率 D.改变压强对反应速率无影响
17.下述实验能达到预期目的的是( )
|
编号 |
实验内容 |
实验目的 |
|
A |
将SO2通入酸性KMnO4溶液中 |
证明SO2具有氧化性 |
|
B |
将锌粒与稀HNO3反应 |
制备H2 |
|
C |
将铜与浓硝酸反应生成的气体收集后用冰水混合物冷却降温 |
研究温度对化学平衡的影响 |
|
D |
分别向2支试管中加入相同体积不同浓度的H2O2溶液,再向其中1支加入少量MnO2 |
研究催化剂对H2O2分解速率的影响 |
16. 同周期的X、Y、Z三种元素的最高价氧化物对应水化物的酸性由强到弱的顺序是:HZO4 H2YO4
H2YO4 H3XO4,下列判断正确的是( )
H3XO4,下列判断正确的是( )
①阴离子的还原性按X、Y、Z顺序减弱 ②单质的氧化性按X、Y、Z顺序增强
③元素的原子半径按X、Y、Z顺序减小 ④气态氢化物的稳定性按X、Y、Z顺序减弱
A.①② B.②③ C.①②③ D.①②③④
15. 下列叙述中,金属a的活泼性肯定比金属b的活泼性强的是( )
A.a原子的最外层电子数比b原子的最外层电子数少
B.a原子电子层数比b原子的电子层数多
C.1mol a 从酸中置换氢生成的H2比1 mol b从酸中置换氢生成的H2多
D.常温时,a能从水中置换出氢,而b不能
14. 下列递变规律不正确的是( )
A.Na.Mg、Al还原性依次减弱 B.I2、Br2、Cl2氧化性依次增强
C.C、N、O原子半径依次增大 D.P、S、Cl最高正价依次升高
13.一定温度下,反应N2(g)+3H2(g)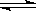 2NH3(g)达到化学平衡状态的标志是( )
2NH3(g)达到化学平衡状态的标志是( )
A.N2、H2和NH3的物质的量分数不再改变
B.c(N2)∶c(H2)∶c(NH3)=1∶3∶2
C.N2与H2的物质的量之和是NH3的物质的量2倍
D.单位时间里每增加1molN2,同时增加3molH2
12.在 错误!不能通过编辑域代码创建对象。 中,m、n、p、q表示X的四个角码,若X1和X2的q均为1,m、p的值相等且P≠0,则X1和X2表示的可能是( )
A.不同种元素的原子 B.同种元素的不同种原子
C.同种元素不同种原子形成的离子 D.不同元素的离子
11.设NA为阿佛加德罗常数,下列叙述中正确的是( )
A.常温常压下,22.4 L CO2和O2混合气体中含有的氧原子数约为2NA
B.常温常压下,0.1 mol Fe在0.1 mol Cl2中充分燃烧,转移的电子数为0.3NA
C.2 mol SO2和1 mol O2混合在(V2O5存在的条件下)密闭容器中加热反应后,容器内物质的分子数大于2NA
D.138克K2CO3晶体中的离子总数大于3NA
10.A和M 为两种主族元素,已知A位于短周期,且A2-与M+的电子数之差为8,则下列说法一定正确的是( )
A、A和M原子的电子总数之和为11
B、A和M的原子序数之差为8
C、A和M原子的最外层电子数之和为7
D、A和M原子的最外层电子数之差为7
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com