
题目列表(包括答案和解析)
22、(8分)以A为原料在化学工业上可制备多种物质,其中的一部分如图所示。A、B、D、E、G的焰色反应均呈黄色,A是由同周期元素组成的离子化合物,其水溶液呈中性,E的水溶液呈强碱性。常温下,X2为黄绿色气体。当G转化为D或E时,同时生成能支持燃烧的无色气体Y2。
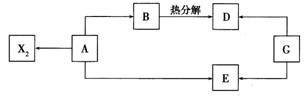
试回答下列问题:
(1)G的电子式为 ,E中的化学键类型为 。
(2)G→D的化学方程式为 。
(3)D在工业上可用于减轻含硫燃料燃烧时的SO2污染。将D粉末与燃料一起喷进燃炉,D与SO2反应产生固体(该固体可进一步被氧化),反应的化学方程式为
。
(4)在X、Y两种元素组成的某种化合物中,Y元素的质量分数为47.4%。该化合物与NaOH反应生成两种含氧酸盐,其中X的化合价分别为+3价和+5价,反应的化学方程式为 。
21、(8分)已知A、B、C、D四种短周期元素原子序数依次增大,并依C、D、B、A顺序原子半径逐渐减小。且知A、C同主族,B、D同主族;B、D两原子核外电子数之和为A、C的原子核外电子数之和的两倍;C元素与其它三种元素均能形成离子化合物。
试回答下列问题:
(1)写出有关化学用语:①D元素的原子结构示意图 ;②A、B形成的化合物A2B2的电子式 。
(2)写出两种均含A、B、C、D四种元素的化合物相互间发生反应且生成气体的离子方程式为 。
(3)a、b、c、d、e五种常见共价化合物分子分别由上述四种元素中的两种构成,其中只有a、c、d为三原子分子,c和e分子中原子核外电子数相同,且知a、e均具有漂白性,b、c两分子以一定比例混合共热可得a、d两种分子,试写出有关化学反应方程式:
①a+e
②b+c→a+d
20、(3分)有一无色透明澄清溶液,可能含有较大量的Cu2+、Ba2+、SO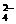 、Cl-、I-、S2-、H+、K+等离子中两种或多种,做如下实验:
、Cl-、I-、S2-、H+、K+等离子中两种或多种,做如下实验:
①取溶液少量加入铁粉有气体放出;②另取原溶液加过量Na2SO3溶液后有气体放出,也有白色沉淀生成,再加硝酸沉淀不消失;③另取原溶液加入AgNO3溶液有白色沉淀生成。由此判断原溶液中一定含有的离子是 ,一定不含有的离子是 ,可能含有的离子是 。
19、(3分)某实验小组为探究ClO-、I2、SO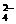 在酸性条件下的氧化性强弱,设计实验如下:
在酸性条件下的氧化性强弱,设计实验如下:
实验①:在淀粉碘化钾溶液中加入少量次氯酸钠溶液,并加入少量的稀硫酸,溶液立即变蓝;
实验②:向实验①的溶液中加入4mL 0.5mol/L的亚硫酸钠溶液,蓝色恰好完全褪去。
(1)写出实验①中发生反应的离子方程式 。
(2)实验②中化学反应转移电子的物质的量是 。
(3)以上实验说明,在酸性条件下ClO-、I2、SO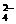 的氧化性由弱到强的顺序是
的氧化性由弱到强的顺序是
。
18、 在某状况下,H2S和CS2的混合气体在足量O2中充分燃烧,生成的SO2的物质的量是CO2的n倍(n>2)(已知CS2+3O2 CO2+2SO2),则原混合物中,H2S和CS2的体积比为 ( )
在某状况下,H2S和CS2的混合气体在足量O2中充分燃烧,生成的SO2的物质的量是CO2的n倍(n>2)(已知CS2+3O2 CO2+2SO2),则原混合物中,H2S和CS2的体积比为 ( )
A、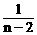 B、
B、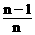 C、
C、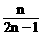 D、n-2
D、n-2
17、将0.03mol Cl2缓缓通入含0.02mol H2SO3和0.02mol HBr的混合溶液中,在此过程中,
溶液中的c(H+)与Cl2用量(物质的量n)的关系示意图是(溶液的体积视为不变)
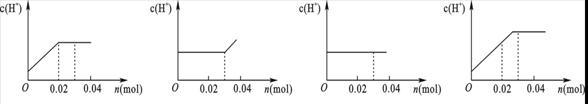 ( )
( )
A B C D
16、将质量分数分别为50%、10%的硫酸溶液等体积混合,所得溶液中硫酸的质量分数
( )
A、大于30% B、小于30% C、等于30% D、无法判断
15、科学家预言超级原子的发现将会重建周期表,2005年1月美国科学家在《Science》上发表论文,宣布发现A1的超原子结构Al13和Al14,并在质谱仪检测到稳定的Al13I-等。Al13、Al14的性质很像现在周期表中的某主族元素,已知这类超原子当具有40个价电子时最稳定。下列说法不正确的是 ( )
A、Al14与ⅡA族元素性质相似
B、Al13与卤素性质类似
C、Al13在气相中与HI反应的方程式可表示为:Al13+HI=HAl13I
D、Al13超原子中Al原子间是通过离子键结合的
14、下列反应中,调节反应物的用量或浓度,不会改变反应产物的是 ( )
A、硫化氢在氧气中燃烧 B、铜在硫蒸气中燃烧
C、二氧化硫通入石灰水中 D、硫酸中加入锌粉
13、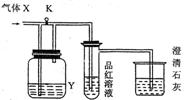 右图是一套检验气体性质的实验装置。向装置中缓缓通入气体X,若关闭活塞K,则品红溶液褪色。据此判断气体X和洗气瓶内的溶液
右图是一套检验气体性质的实验装置。向装置中缓缓通入气体X,若关闭活塞K,则品红溶液褪色。据此判断气体X和洗气瓶内的溶液
Y可能的组合是 ( )
|
|
A |
B |
C |
D |
|
X |
硫化氢 |
二氧化硫 |
二氧化碳 |
氯化氢 |
|
Y |
稀硫酸 |
饱和NaHCO3 |
Na2SO3溶液 |
饱和NaHSO3 |
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com