
题目列表(包括答案和解析)
2、(8分) P (s)和 Cl2(g)发生反应生成 PCl3(g)和 PCl5(g)。反应过程和能量关系如图所示(图中的△H表示生成 l mol 产物的数据)。
根据上图回答下列问题:
(1)P和Cl2反应生成PC13的热化学方程式是 。
(2)PC15分解成 PC13和Cl2的热化学方程式是 ;上述分解反应是一个可逆反应。温度Tl时,在密闭容器中加人0.80 nol PC15 ,反应达平衡时PC15还剩0.60 mol ,其分解率 al等于 ;若反应温度由Tl升高到T2,平衡时PC15的分解率为a2,a2 al(填“大于”、“小于”或“等于”)。
(3)工业上制备PC15通常分两步进行,先将P和C12反应生成中间产物PC13,然后降温,再和Cl2反应生成PCl5。原因是 。
(4)P和C12分两步反应生成1 mol PC15的△H3== ,一步反应生成1 molPC15的△H4____________△H3(填“大于”、“小于”或“等于”)。
(5)PC15与足量水充分反应,最终生成两种酸,其化学方程式是:
。
陕西省西安铁一中08-09学年高一下学期期中考试答题卡
1、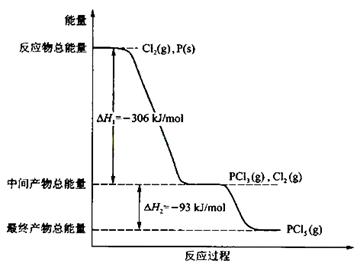 (2分)已知反应32S和H236SO4(浓)在加热的条件下反应,请求出该反应中生成的SO2的摩尔质量:
。
(2分)已知反应32S和H236SO4(浓)在加热的条件下反应,请求出该反应中生成的SO2的摩尔质量:
。
28、(M1和M2选做,M3不做)在5L的密闭容器中充入2molA气体和1molB气体,在一定条件下发生反应:2A(g)+B(g)  2C(g),经4 s后达到平衡状态,在相同温度下测得容器内混合气体的压强是反应前的5/6,
2C(g),经4 s后达到平衡状态,在相同温度下测得容器内混合气体的压强是反应前的5/6,
(1)以B表示的该反应的速率;
(2)达到平衡时,A的转化率
附加题(M3模块必做,M1和M2模块选做)
27、(M3模块必做,M1和M2选做)合成氨工厂常通过测定反应前后混合气体的密度来确定氨的转化率。某工厂测得合成塔中(即合成前)N2、H2混合气体的密度为0.5536g/L(标准状况),从合成塔中出来的混合气体在相同条件下密度为0.693g/L。
求(1)反应前混合气体的物质的量之比;
(2)该合成氨厂N2的转化率。
注意:26题为必做题;27题M3模块必做;27,28题M1和M2模块任选一题,若两题全做,以27题计分。
26、(必做题)某核素ZAX的氯化物XCl2 0.95g配成溶液后,需用1mol/L的硝酸银溶液20mL才能把氯离子完全沉淀下来,试计算:
(1)X的质量数。
(2)若X的核内中子数为12,求47.5gXCl2中所含质子的物质的量是多少?
25、(3分)把6molA气体和5molB气体混合后放入2L密闭容器中,在一定条件下发生反应:3A(气)+B(气)  2C(气)+ xD(气)在5s末时生成2molC,测得D的平均反应速率为0.1mol/L·s。则X= 。A的平均反应速率为
。5s末时B的物质的量浓度是
。
2C(气)+ xD(气)在5s末时生成2molC,测得D的平均反应速率为0.1mol/L·s。则X= 。A的平均反应速率为
。5s末时B的物质的量浓度是
。
24、 (4分)某温度时,在一个2L的密闭容器中,X、Y、Z三种物质
(4分)某温度时,在一个2L的密闭容器中,X、Y、Z三种物质
的物质的量随时间的变化曲线如图所示。根据图中数据,试
填写下列空白:
(1)该反应的化学方程式为 ;
(2)从开始至2min,Z的平均反应速率为 ;
(3)若X、Y、Z均为气体,反应达平衡时:
此时体系的压强是开始时的 倍。
23、(4分)炒过菜的铁锅未及时洗净(残液中含有氯化钠),第二天便出现红棕色的锈斑
[该锈主要成分为Fe(OH)3失水后的产物]。试用有关的电极反应式、化学方程式表示
Fe(OH)3的生成。
负极: 正极:
Fe(OH)3的生成: 。
22、 (13分)A、B、C、D、E五种短周期元素,其原子序数呈递增顺序,A、D同族,B、C同周期,A、B组成的化合物甲为气态,是海底深处“可燃冰”的主要成分,其中A、B原子个数之比为4:1,A元素可形成最轻的气体,由A、C组成的两种化合物乙和丙都为液态,乙中A、C原子个数为1:1,丙中原子数之比为2:1,由D、C组成的2种化合物丁和戊都固态且焰色反应都为黄色,丁中D、C原子个数之比为1:1,戊中原子数之比为2:1,E是地壳中含量最多的金属元素。
(1)写出化学式:
甲 丙
写出下列物质的电子式:
乙 丁 戊
(2)写出D、E最高价氧化物对应水化物相互反应的离子方程式
。
(3)用电子式表示D2C的形成过程:
用电子式表示BC2的形成过程:
(4)B、D、E最高价氧化物对应水化物中,按酸性减弱,碱性增强的顺序排列(写化学式) 。
21、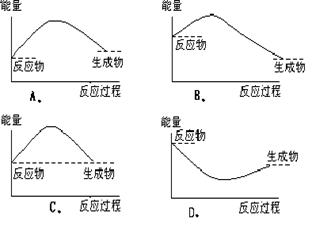 (6分)右侧四幅图中,表示吸热反应的图是 ;请从化学反应实质的角度解释吸热反应
,请举例写出两个吸热反应的化学方程式
,
(6分)右侧四幅图中,表示吸热反应的图是 ;请从化学反应实质的角度解释吸热反应
,请举例写出两个吸热反应的化学方程式
,
。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com