
题目列表(包括答案和解析)
11.下列物质性质变化规律与化学键键能无关的是:
①HF、HCl 、HBr、HI的热稳定性依次减弱 ②NH3易液化
③F2、C12、Br2、I2的熔、沸点逐渐升高 ④H2S的熔沸点小于H2O的熔、沸点
⑤NaF、NaCl、NaBr、NaI的熔点依次减低
A.①③④ B.③④ C.②③④ D.全部
10.下列有关化学键与晶体结构说法正确的是:
A.两种元素组成的分子中一定只有极性键
B.离子化合物的熔点一定比共价化合物的高
C.非金属元素组成的化合物一定是共价化合物
D.含有阴离子的化合物一定含有阳离子
9.设NA表示阿伏加德罗常数的值,下列说法正确的是:
A.由2H和18O所组成的水11g,其中所含的中子数为5NA
B.标准状况下,22.4L CH4中所含C-H键数为4NA
C.在1L0.1mol/L的CH3COOH溶液中,所含CH3COOH分子数为0.1NA
D.1 mol 二氧化硅晶体中含Si-O键的数目为4 NA
8. 晶胞是构成晶体的基本重复单元。在二氧化硅晶胞中有8个硅原子位于立方晶胞的8个顶角,有6个硅原子位于晶胞的6个面心,还有4个硅原子与16个氧原子在晶胞内构成4个硅氧四面体,它们均匀错开排列于晶胞内。根据图示二氧化硅晶胞结构,每个晶胞内所含“SiO2”基元数为 :
晶胞是构成晶体的基本重复单元。在二氧化硅晶胞中有8个硅原子位于立方晶胞的8个顶角,有6个硅原子位于晶胞的6个面心,还有4个硅原子与16个氧原子在晶胞内构成4个硅氧四面体,它们均匀错开排列于晶胞内。根据图示二氧化硅晶胞结构,每个晶胞内所含“SiO2”基元数为 :
A.4个 B.6个 C.8个 D.18个
7. 石墨是层状晶体,每一层内碳原子结构如图所示,如果将每对相邻原子间的化学键看成是一个化学键,则石墨晶体每一层内碳原子数与碳-碳化学键数目的比是:
石墨是层状晶体,每一层内碳原子结构如图所示,如果将每对相邻原子间的化学键看成是一个化学键,则石墨晶体每一层内碳原子数与碳-碳化学键数目的比是:
A.1∶1 B.1∶2 C.1∶3 D.2∶3
6.下列化学用语表示正确的是:
A.钾原子结构示意图: B.CCl4的电子式:
B.CCl4的电子式:
C.HClO的结构式:H-Cl-O
D.MgCl2的电子式: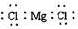
5.有关等物质的量的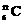 原子和
原子和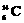 原子,下列叙述中,正确的是:
原子,下列叙述中,正确的是:
①含有相同数目的原子②含有相同物质的量的质子③属于同种元素④具有相同的质量 ⑤中子数相等⑥电子数相等⑦完全燃烧消耗氧气的质量相等⑧具有几乎相同的化学性质
A.只有①②③ B.只有②③⑤ C.除④⑤外都正确 D.全正确
4.若某基态原子的外围电子排布为4d15s2,则下列说法正确的是:
A.该元素位于周期表第5周期第IB族 B.该元素原子核外有5个电子层
C.该元素原子最外层共有3个电子 D.该元素原子M层上共有8个电子
3.下列各组物质熔点高低的比较,正确的是:
A.晶体硅>金刚石>碳化硅 B.CsCl>KCl>NaCl
C.SiO2>CO2>He D.Br2> I2>He
2.下列叙述中正确的是:
A.同周期元素中,ⅦA族元素的原子半径最大
B.ⅥA族元素的原子,其半径越大,越容易得到电子
C.当各轨道处于全满、半满、全空时原子较稳定
D.同一周期中,碱金属元素的第一电离能最大
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com