
题目列表(包括答案和解析)
20. (11分)A、B、C、D均
为中学化学比较常见的物质。
它们间的反应关系如右图所
示。(如有必要,可以适当加
热)
(1)若A为元素周期表中第
三周期活泼的金属元素的单质,B为A1C13,则反应后的无色溶液D中必含有的溶质是
,(填相应的化学式)。可能还含有其它溶质,将可能还含有其它的溶质及要检验其存在所用的试剂和实验现象填入下表(根据实际情况可填满,也可不填满,甚至可以补充。)
|
编号 |
可能有的溶质 |
检验试剂 |
实验现象 |
|
1 |
|
|
|
|
2 |
|
|
|
|
3 |
|
|
|
(2)若A是常见的可溶性强碱,B是一种酸式盐,D是水,则白色沉淀可能是 (任
写一种);当生成的沉淀不溶于盐酸时,写出过量A与B反应的离子方程式 。
(3)若B是A12(SO4)3,A、E既可与盐酸反应,又可与NaOH溶液反应,气体C能使澄清石灰水变浑浊的无色无味的气体,D溶液的焰色反应为黄色。则A为 。
19.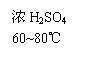 (6分)已知甲酸和浓硫酸共热到60~80℃可发生脱水反应:
(6分)已知甲酸和浓硫酸共热到60~80℃可发生脱水反应:
HCOOH----→ CO↑+H2O
实验室用甲酸和浓硫酸混和后制取CO时,常不需加热,其具体操作方法如下:在试管内倒入一定体积的甲酸,然后再小心沿试管壁倒入等体积的浓硫酸,这时可见试管内液体分上、下两层,在两层液体的界面处有少量气泡,轻轻振动试管,可见液体交界面气泡增多,改变振动的力度可控制气泡产生的速率。试回答下列问题
(1)用该法制CO不需加热的原因: 。
 (2)以上操作方法可控制反应速率的原因:
。
(2)以上操作方法可控制反应速率的原因:
。
(3)具支试管(试管侧壁有一支管,如右图所示)在实验室有多种用途,试只用具支试管、橡皮塞(橡皮塞上最多只能打一个孔)、玻璃导管及连接和夹持仪器装配一个用浓硫酸和甲酸的混合液制取CO气体,用CO还原氧化铜,并检验其氧化产物的实验装置。画出该装置示意图(同类仪器最多只有三件,不必画夹持仪器,但需注明所装的药品)

18.有一包白色固体,可能有①(NH4)2SO4,②Al2(SO4)3,③NaCl,④AgNO3,⑤KOH,⑥KI,⑦BaCl2中的一种或几种组成,该固体溶于水得到澄清溶液,而且该溶液能使酸酞呈红色,若在该溶液中加入适量的稀硝酸,可得到白色沉淀。该白色固体可能的组成是
A.②③⑤ B.②⑤⑦ C.①③④⑤ D.①④⑤⑦
17.液态锂离子电池是指Li+嵌入化合物为正负电池的二次电池。正极采用锂化合物LiCoO2,负极采用碳电极,充电后成为锂-碳层间化合物LixC6(0<x≤1),电解质为溶解有锂盐LiPF6、LiAsF6等的有机溶液。下列有关说法不正确的是
A.将LiCoO2改写成为氧化物的形式为Li2O·Co2O3
B.该电池的电解液必须使用有机溶剂主要是由于有机溶剂有良好的导电性
C.Li是3号元素,是最轻的金属之一,这类电池比能量高
D.在电池充、放电时,Li+在两个电极之间往返嵌入和脱嵌。该电池的充放电反应方程式为:
 LiCoO2+6C
Li1-xCoO2+LixC6
LiCoO2+6C
Li1-xCoO2+LixC6
16.如图所示,将紧紧缠绕不同金属的铁钉放入培养皿中,再加入含有适量酚酞和NaCl的琼脂热溶液,冷却后形成琼胶(离子在琼胶内可以移动),下列叙述正确的是
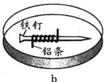
 A.b中铁钉附近呈现红色
A.b中铁钉附近呈现红色
B.b中铁钉上发生还原反应
C.a中铜丝上发生氧化反应
D.b中铝条附近有气泡产生
15.下列有关电化学的图示中,完全正确的是
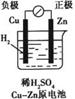
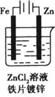
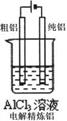
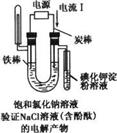
A B C D
14.对于以下反应:A(s)+3B(g) 2C(g)+D(g),在一定温度、压强下,在一体积可变的容器中,当下列物理量不再发生变化时就可确定一定达到平衡状态的是
A.容器的体积不再发生变化 B.B的生成速率和D的生成速率为3∶1
C.混合气体的密度不随时间变化 D.B、C、D的分子数之比为3∶2∶1
13.下列离子方程式正确的是
A.氯化银可被NaCN溶液所溶解:AgC1+2CN-=[Ag(CN)2]-+C1-
B.亚磷酸是一种二元酸,在其中加入过量的烧碱溶液:H3PO3+3OH-=PO33-+3H2O
C.硫酸亚铁和稀硫酸的混合溶液中滴入双氧水:Fe2++H2O2+H+=Fe3++H2O
 D.偏铝酸钠和等物质的量的硫酸反应:3AlO2-+6H+==Al3++2Al(OH)3
D.偏铝酸钠和等物质的量的硫酸反应:3AlO2-+6H+==Al3++2Al(OH)3
12.已知次氯酸分子的结构式为H-O-Cl,下列有关说法正确的是
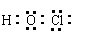 A.O原子发生sp杂化
B.O原子与H、Cl都形成σ键
A.O原子发生sp杂化
B.O原子与H、Cl都形成σ键
C.该分子为直线型分子 D.该分子的电子式是
11.设NA代表阿伏加德罗常数的数值,下列说法中正确的是
①常温常压下,9g甲烷(14CH4)所含的中子数为5NA
②常温常压下,22.4L N2气体的分子数小于NA
③64g的铜发生氧化还原反应,一定失去2NA个电子
④常温常压下,100mL 0.5mol/L的醋酸溶液中,醋酸的分子数目小于0.05NA
⑤标准状况时,22.4LSO3所含有的分子数为NA
⑥常温常压下,lmol氦气分子含有的核外电子数为4NA
A.①② B.③④ C.②④ D.⑤⑥
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com