
题目列表(包括答案和解析)
5、在2A+B ==== 3C+4D反应中,表示该反应速率最快的是
A.υ(A)=0.5 mol·(L·s)-1 B.υ(B)=0.3 mol·(L·s)-1
C.υ(C)=0.8 mol·(L·s)-1 D.υ(D)=1 mol·(L·s)-1
4、下列关于物质性质的比较,不正确的是
A.酸性强弱:HIO4 >HBrO4> HClO4
B.原子半径大小:Na> S >O
C.热稳定性:HCl>H2S>PH3>AsH3
D.碱性强弱:KOH > NaOH > LiOH
3、已知碳有三种常见的同位素:12C、13C、14C,氧也有三种同位素:16O、17O、18O,由这六种微粒构成的二氧化碳分子中,其相对分子质量最多有
A.18种 B.6种 C.7种 D.12种
2、科学家预测:人类将在21世纪大量使用氢气作燃料。其中最理想获得氢气的途径是
A.以焦炭和水制取水煤气后分离出氢气
B.用铁、锌等活泼金属与稀硫酸反应制取氢气
C.由火力发电厂提供电力电解水产生氢气
D.利用高效催化剂和太阳能使海水分解产生氢气
1、“嫦娥一号”成功发射,标志着我国实施绕月探测工程迈出重要一步。其任务之一是探测月球土壤厚度、探明氦-3(3He)储量。下列有关氦-3的说法中正确的是
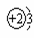 A.原子结构示意图为 B.原子核内中子数为3
A.原子结构示意图为 B.原子核内中子数为3
C.1mol3He的质量约为3g D.3He的摩尔质量为3
25.(6分)在酸溶液中,10.00g Cu2S和CuS的混合物与250.0mL 0.7500 mol·L-1的MnO4-反应生成了SO42-、Cu2+和Mn2+。剩余的MnO4-恰好与175.0mL浓度为 1.000 mol·L-1的Fe2+ 溶液反应。
(1)分别写出Cu2S、CuS与酸性KMnO4溶液反应的离子方程式,并配平。
(2)试计算原始混合物中 CuS 的质量分数。
24.(5分)在少量水存在下,使9.8g的固体物质A和3.6 g的固体物质B反应,生成了4.48L气态产物C(标况下),该气体的密度为0.759g/L。将同样多的物质A同过量2倍的氢氧化钙一起加热,产生1.70g气体,向3.6g物质B中逐滴加入氢溴酸直至反应终止,同样生成1.70g气体。若已知在三种情况下,均生成了同一气态和固态产物,由此推知:
(1)A是 ,B是 ,C是
(2)写出化学方程式:A和B
23. (9分)铜及其合金是人类最早使用的金属材料。
(9分)铜及其合金是人类最早使用的金属材料。
(1)铜原子的核外电子排布式是 。
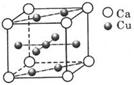
(2)如图是金属Ca和Cu所形成的某种合金的晶胞结构示意图,则该合
金中Ca和Cu的原子个数比为 。
(3)Cu2+能与NH3、H2O、C1-等形成配位数为4的配合物。
①[Cu(NH3)4]2+具有对称的空间构型,[Cu(NH3)4]2+中的两个NH3被两个Cl-取代,能得到两种不同结构的产物,则[Cu(NH3)4]2+的空间构型为 。
②某种含Cu2+的化合物可催化丙烯醇制备丙醛的反应:HOCH2CH=CH2→CH3CH2CHO。在丙烯醇分子中发生某种方式杂化的碳原子数,是丙醛分子中发生同样方式杂化的碳原子数的2倍,则这类碳原子的杂化方式为 。
(4)CaO晶体的结构与NaCl相同,CaO晶体中Ca2+的配位数为 。
晶格能分别为:CaO为-3401 kJ·mol-1、NaCl为-786 kJ·mol-1。导致两者晶格能差异的主要原因是 。
(5)假定铁有简单立方、体心立方(bcp)、面心立方(ccp)三种同素异形体,三种晶体在不同温度下能发生相互转化。若三种同素异形体晶胞边长分别为a cm, b cm,c cm则三种晶体密度比为 。
22.(11分)利用燃料和氧化剂之间发生的氧化还原反应,将化学能直接转化为电能的装置叫燃料电池,它是一种高效低污染的新型电池。燃料电池所用燃料可以是氢气,也可以是甲烷、甲醇、肼、氨等。肼分子(H2N-NH2)可以在氧气中燃烧生成氮气和水,回答下列问题:
(1)利用肼、氧气与KOH溶液组成碱性燃料电池,请写出该电池负极的电极反应式:
,并指出电解质溶液中OH-离子向 极移动。
若用该燃料电池电解饱和食盐水得C12 7.1g,则需肼 g,若想将电解后饱和食盐水恢复原状,需 。
(2)用电离方程式表示肼的水溶液呈碱性的原因 ;
(3)天然气有着来源广,污染小的优点,但未能在汽车燃料中推广应用,而其催化氧化产物甲醇却被推广使用,主要是因为 。
(4)如果将燃料改为汽油则为汽油燃料电池,该燃料电池最大的障碍是氧化反应不完全产生
堵塞电极的气体通道,有人估计,完全避免这种副反应至少还需10年时间,正是新一代化学家的历史使命。
(5)肼是强还原剂,与氧化剂H2O2反应时可放出大量的热,因此,肼可以作为火箭推进剂。
某些共价键的键能
|
键 |
键能/kJ·mol-1 |
键 |
键能/kJ·mol-1 |
键 |
键能/kJ·mol-1 |
|
N-N |
193 |
N=N |
418 |
N≡N |
946 |
|
O-O |
142 |
O=O |
497 |
H-H |
436 |
|
N-H |
391 |
O-H |
463 |
|
|
根据以上信息,试写出肼与H2O2反应的热化学方程式 。
21. (8分)某研究性学习小组成员,利用稀硫酸与某金属的反应来探究影响化学反应速率的因素,下表是研究过程中记录的实验数据:(表中某些数据记录已模糊不清,个别数据已丢失。)
 实验 实验序号 |
金属 质量/g |
金属 状态 |
c(H2SO4) /mol·L-1 |
v(H2SO4) /mL |
溶液温度/°C |
金属消失的时间/s |
|
|
1 |
0.10 |
丝 |
0.5 |
50 |
20 |
34 |
500 |
|
2 |
0.10 |
粉末 |
0.5 |
50 |
20 |
35 |
50 |
|
3 |
0.10 |
丝 |
0.7 |
50 |
20 |
36 |
数据模糊 |
|
4 |
0.10 |
丝 |
0.8 |
50 |
20 |
35 |
200 |
|
5 |
0.10 |
粉末 |
0.8 |
50 |
20 |
36 |
数据模糊 |
|
6 |
0.10 |
丝 |
1.0 |
50 |
20 |
35 |
数据模糊 |
|
7 |
0.10 |
丝 |
1.0 |
50 |
35 |
数据模糊 |
50 |
|
8 |
0.10 |
丝 |
1.1 |
50 |
20 |
34 |
100 |
|
9 |
0.10 |
丝 |
1.1 |
50 |
数据丢失 |
44 |
40 |
若实验操作、数据记录均是正确的,请分析上述数据,回答下列问题:
(1)该实验主要是探究 因素对反应速率的影响。
(2)经仔细辨认,模糊的数据疑为25、50、125、250,试将这些疑似数据填入表中,使实验数据较为合理。
(3)试猜测实验9反应前溶液的温度约为 °C。推测的依据是 。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com